��Ŀ����
12��ͼ��A��B��C�ֱ��������л���Ľṹģ�ͣ�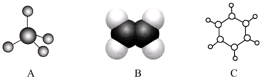
��ش��������⣺
��1��A����ͬϵ��ķ���ʽ����ͨʽCnH2n+2����n=4ʱ��������ʼ����ͬ���칹�壮
��2��A��B��C�����л����У�����ԭ�Ӿ����������ϩ�ͱ��������ƣ���
��3���л���C���еĽṹ��������bd������ĸ����
a����̼̼˫����̼̼��������Ľṹ
b���ж���������ˮ���ܶȱ�ˮС
c������ʹ����KMnO4��Һ����ˮ��ɫ
d��һ������������������������Ӧ
��4���������������л�����ȫȼ������H2O��CO2�������������������ͬ״���£�������CH4�������ʽ����
���� ��ͼ��֪��A�к�1��C��4��H��ΪCH4��Ϊ��������ṹ����B�к�2��C��4��H����ΪCH2=CH2��Ϊƽ��ṹ���ҷ����ӳɡ�������Ӧ��C�к�6��C��6��H��ΪC6H6��Ϊƽ���������Σ�����˫��������ȡ�������ܱ����������������ϵ�����ʱ���л��ﺬ����Խ��ȼ��ʱ��������Խ�������
��� �⣺����������ͨʽΪCnH2n+2���Ӷ�������ʼ����ͬ���칹�壬���Դ�n=4��ʼ����ͬ���칹�壬�ʴ�Ϊ��CnH2n+2��4��
��2��A�Ǽ��顢B����ϩ��C�DZ�����������������ṹ����ϩ�ͱ�����ƽ��ṹ��������ϩ�ͱ�������ԭ�ӹ�ƽ�棬�ʴ�Ϊ����ϩ�ͱ���
��3�����C�DZ���
a���÷����в�����̼̼������˫�����ǽ��ڵ�����˫��֮����������м����ʴ���
b�����ж���������ˮ���ܶȱ�ˮС�����Ժ�ˮ��Ϸֲ㣬ˮ���²㣬����ȷ��
c�������ʽ��ȶ���������KMnO4��Һ����ˮ����Ӧ��������ȡ��ˮ�е����ʹ��ˮ��ɫ���ʴ���
d��һ���������������������ӳɷ�Ӧ���ܺ���������������Ӧ������ȷ��
�ʴ�Ϊ��bd��
��4��������ʱ���л��ﺬ����Խ��ȼ��ʱ��������Խ�ࣻ�������ʵ����ʽ�ֱ�ΪCH4��CH2��CH����ȻCH4�������������ʱ������O2��࣬
�ʴ�Ϊ��CH4��
���� ���⿼���л���Ľṹ�����ʣ����������Լ��顢��ϩ����Ϊ������������ϩ��������ͬϵ������ʺͽṹ��֪��������Ӧ�����ͣ�ע�ⱽ����ˮ����Ӧ������ȡ�壬Ϊ�״��㣮

 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�| A�� | �ڱ�״���£�22.4Lˮ������ԼΪ18g | |
| B�� | 1.7g��������ԭ����ĿΪ0.4NA | |
| C�� | ͬ��ͬѹʱ����ͬ������κ����嵥��������ԭ������ͬ | |
| D�� | 1 L 1mol•L-1��Na2SO4��Һ�к�Na+�ĸ���ΪNA�� |
| A�� | NH3•H2O�ĵ��뷽��ʽ��NH3•H2O�TNH4++OH- | |
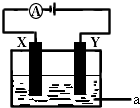
| B�� | ������������ʴ��������Ӧ��O2+2H2O+4e-�T4OH- | |
| C�� | ̼����ˮ������ӷ���ʽ��CO32-+2H2O�T2OH-+H2CO3 | |
| D�� | �����ȼ������890kJ/mol�������ȼ�յ��Ȼ�ѧ����ʽ��CH4��g��+2O2��g���TCO2��g��+2H2O��g����H=+890kJ/mol |
| A�� | ������Ԫ���γ�XY2�ͻ��������XY2���γɷ��Ӿ��壬��XY2�ǷǼ��Է��� | |
| B�� | ������Ԫ���γ�YX2�ͻ������YX2�ȿ����γ�ԭ�Ӿ��壬Ҳ�����γɷ��Ӿ��� | |
| C�� | ������Ԫ�ؿ��γ�YX�ͻ������YX�ľ���һ���������Ӿ��� | |
| D�� | ������Ԫ�ؿ��γ�YX3�ͻ������YX3��ˮ��Һ���ܳ�ǿ���� |



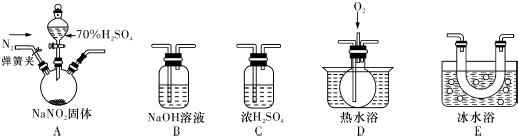
 ��1��ʵ��֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���C��
��1��ʵ��֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���C��