题目内容
17.周期表前四周期的元素Q、R、X、Y、Z原子序数依次增大,Q元素的原子形成的离子就是一个质子:R基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,X基态原子s能级的总电子数比p 能级的总电子数多1:Y原子的核外成对电子数是未成对电子数的3倍:Z原子的价电子排布为3d74S2回答下列问题:
(l)R、X、Y中第一电离能最大的是N(填元素符号),其中Y原子的电子排布式为1s22s22p4
(2)Q、R元素形成的某分子中共有14个电子,该分子中R原子采取sp 杂化,该分子的立体构型为直线型
(3)RY可以和很多过渡金属形成配合物,如Fe(RY)5)、Ni(RY)4,其中Fe(RY)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(RY)5晶体属于分子晶体(填晶体类型),RY与N2互为等电子体,与RY互为等电子体的离子有CN-(任写一种)
(4)向含Z2+的溶液中加入过量的氨水,并通入适量的Y2气体,生成有[Z(NH3)6]3+离子则该反应的离子方程式为4Co2++24NH3.H2O+O2=4[Co(NH3)6]3++4OH-+22H2O.
分析 周期表前四周期的元素Q、R、X、Y、Z原子序数依次增大,Q元素的原子形成的离子就是一个质子,则Q为H元素;R基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,核外电子排布式为1s22s22p2,故R为C元素;X基态原子s能级的总电子数比p能级的总电子数多1,核外电子排布式为1s22s22p3,则X为N元素;Y原子的核外成对电子数是未成对电子数的3倍,核外电子排布式为1s22s22p4,则Y为O元素;Z原子的价电子排布为3d74S2,则Z为Co,以此解答该题.
解答 解:周期表前四周期的元素Q、R、X、Y、Z原子序数依次增大,Q元素的原子形成的离子就是一个质子,则Q为H元素;R基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,核外电子排布式为1s22s22p2,故R为C元素;X基态原子s能级的总电子数比p能级的总电子数多1,核外电子排布式为1s22s22p3,则X为N元素;Y原子的核外成对电子数是未成对电子数的3倍,核外电子排布式为1s22s22p4,则Y为O元素;Z原子的价电子排布为3d74S2,则Z为Co,
(1)同周期随原子序数增大,元素第一电离能呈增大趋势,N元素原子2p能级为半满稳定状态,第一电离能高于同周期相邻元素,故第一电离能N>O>C,
Y原子的电子排布式为:1s22s22p4,
故答案为:N;1s22s22p4;
(2)H、C元素形成的某分子中共有14个电子,该分子为C2H2,为直线型结构,该分子中C原子采取 sp杂化,
故答案为:sp;直线型;
(3)Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe (CO)5晶体属于分子晶体,CO与N2互为等电子体,与CO互为等电子体的离子有CN-等,
故答案为:分子晶体;CN-;
(4)向含Co2+的溶液中加入过量的氨水,并通入适量的O2气体,生成有[Co(NH3)6]3+离子,则该反应的离子方程式为:4Co2++24NH3.H2O+O2=4[Co(NH3)6]3++4OH-+22H2O,
故答案为:4Co2++24NH3.H2O+O2=4[Co(NH3)6]3++4OH-+22H2O.
点评 本题是对物质结构与性质的考查,为高考常见题型,涉及核外电子排布、电离能、杂化方式与空间构型判断、等电子体、晶体结构与性质、配合物等,是对学生综合能力的考查.

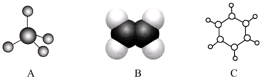
| A. | 苯能使酸性高锰酸钾溶液褪色 | |
| B. | 苯分子具有平面正六边形结构,12个原子在同一平面上,对位上的4个原子在一条直线上 | |
| C. | 苯能使溴水褪色,是发生了取代反应 | |
| D. | 苯不含有碳碳双键故不能发生加成反应 |
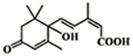 大量盆栽鲜花因施用了S-诱抗素制剂,得以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )
大量盆栽鲜花因施用了S-诱抗素制剂,得以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )| A. | 1mol该物质与足量的NaOH溶液反应最多消耗2mol NaOH | |
| B. | 该物质在Cu作催化剂条件下能被催化氧化 | |
| C. | 该物质能发生氧化、还原、取代反应 | |
| D. | 分别与足量的Na、NaHCO3 反应生成的气体在相同状况下体积比为2:1 |
| A. | 氯气的体积为1.12 L | |
| B. | 原烧碱溶液中含溶质离子0.2NA个 | |
| C. | 所得溶液中含OH-的数目为1×10-5NA | |
| D. | 所得溶液中ClO-的数目为0.05NA |
| A. | 水的电离程度:①<② | |
| B. | ①、②中粒子浓度关系均符合:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) | |
| C. | 将③、④混合,所得溶液的pH>7,则该溶液中:c(NH4+)=c(NH3•H2O) | |
| D. | 向③、④中分别加入25mL0.1mol•L-1盐酸后,溶液中c(NH4+):③=④ |
 .
.