题目内容
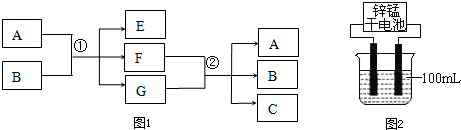
如图是中学化学常见物质的转化关系,其中部分产物未写出,常温下D、N、Y是气体,A、F、N是单质,根据要求回答以下问题:

(1)写出Y的化学式 ,H的电子式 .
(2)收集气体Y的方法是 .
(3)写出A与B反应的离子方程式 .
(4)将过量粉末状H加入到G的水溶液中,能够观察到哪些实验现象? .写出有关反应过程的化学反应方程式 .
(5)有报道说:高温下将F和NaOH反应可得Na.同时还有带磁性的物质生成,写出反应方程式并说明能发生上述反应的原因 .

(1)写出Y的化学式
(2)收集气体Y的方法是
(3)写出A与B反应的离子方程式
(4)将过量粉末状H加入到G的水溶液中,能够观察到哪些实验现象?
(5)有报道说:高温下将F和NaOH反应可得Na.同时还有带磁性的物质生成,写出反应方程式并说明能发生上述反应的原因
考点:无机物的推断
专题:推断题
分析:由题中(5)信息可知,高温下将F和NaOH反应可得Na.同时还有带磁性的物质生成,该磁性物质应为Fe3O4,则F为Fe,A、F为单质,可知F+C→A+G的反应为置换反应,A应是活泼性较铁弱的金属,常见的金属为Cu,则C应为铜盐,可知A与B发生氧化还原反应,由D+N→Y,且Y+E→D+B可知,B应为强氧化性酸,应为HNO3,则C为Cu(NO3)2,D为NO,E为H2O,所以N为O2,Y为NO2,G为Fe(NO3)2,由G+H→M+N可知粉末状H应为Na2O2,则M为Fe(OH)3,结合对应物质的性质以及题目要求解答该题.
解答:
解:由题中(5)信息可知,高温下将F和NaOH反应可得Na.同时还有带磁性的物质生成,该磁性物质应为Fe3O4,则F为Fe,A、F为单质,可知F+C→A+G的反应为置换反应,A应是活泼性较铁弱的金属,常见的金属为Cu,则C应为铜盐,可知A与B发生氧化还原反应,由D+N→Y,且Y+E→D+B可知,B应为强氧化性酸,应为HNO3,则C为Cu(NO3)2,D为NO,E为H2O,所以N为O2,Y为NO2,G为Fe(NO3)2,由G+H→M+N可知粉末状H应为Na2O2,则M为Fe(OH)3,
(1)由以上分析可知Y为NO2,H为Na2O2,电子式为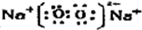 ,故答案为:NO2;
,故答案为:NO2;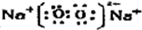 ;
;
(2)Y为NO2,易溶于水,且与水反应,密度比空气大,可用向上排空气法收集,故答案为:向上排空气;
(3)铜和稀硝酸发生氧化还原反应的离子方程式为3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑,故答案为:3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑;
(4)过量过氧化钠加入到硝酸亚铁溶液中,让氧化钠与水反应生成氧气和氢氧化钠,氢氧化钠和硝酸亚铁反应生成氢氧化亚铁,氢氧化亚铁不稳定,易被氧化生成红棕色的氢氧化铁,现象是溶液中先有白色沉淀生成,随即变为灰绿色,最后又变成红褐色沉淀,并产生无色气体,反应的相关方程式为2Na2O2+2H2O=4NaOH+O2↑、Fe(NO3)2+2NaOH=Fe(OH)2↓+2NaNO3、4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:溶液中先有白色沉淀生成,随即变为灰绿色,最后又变成红褐色沉淀,并产生无色气体;2Na2O2+2H2O=4NaOH+O2↑、Fe(NO3)2+2NaOH=Fe(OH)2↓+2NaNO3、4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(5)高温下将F和NaOH反应可得Na.同时还有带磁性的物质生成,应为Fe3O4,高温下反应生成的Na为气体,有利于平衡向正向移动,涉及的反应方程式为3Fe+8NaOH=8Na+Fe3O4+4H2O,故答案为:3Fe+8NaOH=8Na+Fe3O4+4H2O,因为生成气态钠和固态四氧化三铁,化学平衡向右移动.
(1)由以上分析可知Y为NO2,H为Na2O2,电子式为
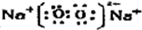 ,故答案为:NO2;
,故答案为:NO2;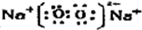 ;
;(2)Y为NO2,易溶于水,且与水反应,密度比空气大,可用向上排空气法收集,故答案为:向上排空气;
(3)铜和稀硝酸发生氧化还原反应的离子方程式为3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑,故答案为:3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑;
(4)过量过氧化钠加入到硝酸亚铁溶液中,让氧化钠与水反应生成氧气和氢氧化钠,氢氧化钠和硝酸亚铁反应生成氢氧化亚铁,氢氧化亚铁不稳定,易被氧化生成红棕色的氢氧化铁,现象是溶液中先有白色沉淀生成,随即变为灰绿色,最后又变成红褐色沉淀,并产生无色气体,反应的相关方程式为2Na2O2+2H2O=4NaOH+O2↑、Fe(NO3)2+2NaOH=Fe(OH)2↓+2NaNO3、4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:溶液中先有白色沉淀生成,随即变为灰绿色,最后又变成红褐色沉淀,并产生无色气体;2Na2O2+2H2O=4NaOH+O2↑、Fe(NO3)2+2NaOH=Fe(OH)2↓+2NaNO3、4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(5)高温下将F和NaOH反应可得Na.同时还有带磁性的物质生成,应为Fe3O4,高温下反应生成的Na为气体,有利于平衡向正向移动,涉及的反应方程式为3Fe+8NaOH=8Na+Fe3O4+4H2O,故答案为:3Fe+8NaOH=8Na+Fe3O4+4H2O,因为生成气态钠和固态四氧化三铁,化学平衡向右移动.
点评:化学推断题是一类综合性较强的试题,如元素及化合物性质和社会生活,环境保护,化学计算等知识,还可引入学科间综合.它不仅可考查学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法.解框图题的方法:最关键的是寻找“突破口”,“突破口”就是抓“特”字,例如特殊颜色、特殊状态、特殊气味、特殊反应、特殊现象、特殊制法、特殊用途等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某有机物中有一个苯环、一个-C3H7、一个-OH,则它属于酚类的结构可能有( )
| A、3种 | B、4种 | C、5种 | D、6种 |
对于Cu、Zn和稀硫酸构成的原电池,下列说法错误的是( )
| A、Zn是负极 |
| B、Cu极上发生氧化反应 |
| C、在外电路中电子由Zn极流向Cu极 |
| D、溶液中,SO42-向Zn极移动 |