题目内容
 纯碱中常含有少量氯化钠,请设计实验测定纯碱中Na2CO3的质量分数.根据你所设计的方案中的有关的数据,写出纯碱中Na2CO3的质量分数的表达式.
纯碱中常含有少量氯化钠,请设计实验测定纯碱中Na2CO3的质量分数.根据你所设计的方案中的有关的数据,写出纯碱中Na2CO3的质量分数的表达式.【实验原理】将纯碱与硫酸反应生成的CO2吸收,测吸收容器增重即知CO2的质量,进而求得纯碱中Na2CO3的质量分数.
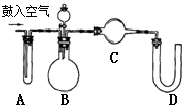
【实验装置】反应装置可用固液(不加热)制气的装置,用碱石灰或固体NaOH吸收CO2气体的装置可用干燥管或U形管.如图所示:
【实验步骤】
a.按上图装置组合好实验仪器,检查气密性;
b.准确称量U型管的质量(设为m1g);
c.准确称量一定量的纯碱(设为ng)放入烧瓶中;
d.打开分液漏斗中活塞,让稀硫酸“缓慢”滴下,至不再产生气体为止;
e.“缓慢”鼓入空气数分钟,然后称U型管总质量(设为m2g).
请你根据上述实验回答下列问题:
(1)A中盛放
(2)D装置所起的作用是
(3)在实验操作e中鼓入空气数分钟的目的是
(4)根据上面数据,可求出纯碱的质量分数为:
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:(1)A装置是吸收空气中的二氧化碳气体避免一下实验测定;
(2)B装置中是纯碱中常含有少量氯化钠,加入稀硫酸反应生成二氧化碳、水蒸气,装置C吸收水蒸气,U形管吸收二氧化碳气体;
(3)在实验操作e中鼓入空气数分钟的目的是把反应生成的二氧化碳气体全部赶入装置C完全吸收;
(4)结合二氧化碳这里和碳元素守恒计算碳酸钠质量分数.
(2)B装置中是纯碱中常含有少量氯化钠,加入稀硫酸反应生成二氧化碳、水蒸气,装置C吸收水蒸气,U形管吸收二氧化碳气体;
(3)在实验操作e中鼓入空气数分钟的目的是把反应生成的二氧化碳气体全部赶入装置C完全吸收;
(4)结合二氧化碳这里和碳元素守恒计算碳酸钠质量分数.
解答:
解:(1)A装置是用氢氧化钠溶液吸收空气中的二氧化碳气体,提供不含二氧化碳气体的气体,用来驱赶装置B中生成的二氧化碳全部进入U形管,避免影响实验测定;
故答案为:NaOH;吸收空气中的二氧化碳,防止影响测定结果;
(2)B装置中是纯碱中常含有少量氯化钠,加入稀硫酸反应生成二氧化碳、水蒸气,装置C吸收水蒸气,U形管吸收二氧化碳气体,称量吸收前后的质量得到二氧化碳质量;
故答案为:测定生成的二氧化碳质量;
(3)在实验操作e中鼓入空气数分钟的目的是把反应生成的二氧化碳气体全部赶入装置D完全吸收;
故答案为:把反应生成的二氧化碳全部赶入装置D中完全吸收;
(4)结合二氧化碳这里和碳元素守恒计算碳酸钠质量分数,二氧化碳物质的量n(CO2)=
mol,纯碱的质量分数=
×100%=
×100%;
故答案为:
×100%.
故答案为:NaOH;吸收空气中的二氧化碳,防止影响测定结果;
(2)B装置中是纯碱中常含有少量氯化钠,加入稀硫酸反应生成二氧化碳、水蒸气,装置C吸收水蒸气,U形管吸收二氧化碳气体,称量吸收前后的质量得到二氧化碳质量;
故答案为:测定生成的二氧化碳质量;
(3)在实验操作e中鼓入空气数分钟的目的是把反应生成的二氧化碳气体全部赶入装置D完全吸收;
故答案为:把反应生成的二氧化碳全部赶入装置D中完全吸收;
(4)结合二氧化碳这里和碳元素守恒计算碳酸钠质量分数,二氧化碳物质的量n(CO2)=
| m2-m1 |
| 44 |
| ||
| n |
| 53(m2-m1) |
| 22 |
故答案为:
| 53(m2-m1) |
| 22 |
点评:本题考查了物质组成和实验测定分析计算.实验过程的理解应用和装置作用的分析判断,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
0.1mol/L氨水中,溶液中随着水量的增加而减少的是( )
A、
| ||
B、
| ||
| C、C(H+)和C(OH-)的乘积 | ||
| D、OH-的物质的量 |
下列能达到实验目的是( )
A、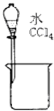 分离水和CCl4 |
B、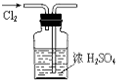 干燥Cl2 |
C、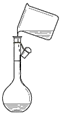 转移溶液 |
D、 蒸发食盐水 |
为达到下列实验目的,所采用的方法正确的是( )
| A、从溴水中提取溴--分液 |
| B、分离水和汽油的混合物--蒸馏 |
| C、从硝酸钾和氯化钾混合液中获取硝酸钾--蒸发 |
| D、分离饱和食盐水和沙子的混合物--过滤 |
浓度均为0.1mol?L-1的五种溶液:①CH3COOH ②NaOH ③CH3COONa ④Ba(OH)2 ⑤Na2CO3中,由水电离出的c(OH-)由小到大的顺序正确的是( )
| A、④②③①⑤ |
| B、②④①⑤③ |
| C、①③⑤②④ |
| D、④②①③⑤ |
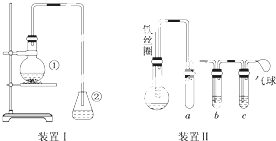 为探究苯与溴的取代反应,甲用如图装置Ⅰ进行如下实验:
为探究苯与溴的取代反应,甲用如图装置Ⅰ进行如下实验: