题目内容
12.下列有关原子核外电子排布的说法中不正确的是( )| A. | 电子总是先排布在能量最低的电子层里 | |
| B. | 每个电子层最多能容纳的电子数为2n2 | |
| C. | 最外层电子数不超过8个(K为最外层时不超过2个) | |
| D. | S2-的M层电子数是K层电子数的3倍 |
分析 A.电子是离核由近到远,能量由低到高依次排布的;
B.每个电子层最多容纳的是2n2个电子;
C.最外层电子数不超过8个(第一层即K层为最外层时,电子数不超过2个);
D.S2-的M层电子数是8个,K层为2个.
解答 解:A.电子是离核由近到远,能量由低到高依次排布的,故A正确;
B.每个电子层最多容纳的是2n2个电子,故B正确;
C.最外层电子数不超过8个,第一层即K层为最外层时,电子数不超过2个,故C正确;
D.S2-的M层电子数是8个,K层为2个,则S2-的M层电子数是K层电子数的4倍,故D错误;
故选D.
点评 本题考查原子构成与核外电子排布规律,难度中等,注意熟练掌握基础知识.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.某气态烃0.5mol能和1mol HCl充分加成,加成产物1mol又能和6mol Cl2完全取代,则该烃是( )
| A. | C2H6 | B. | C2H2 | C. | C3H4 | D. | C4H6 |
7.硝酸被称为“国防工业之母”是因为它是制取炸药的重要原料.下列实验事实与硝酸性质不相对应的一组是( )
| A. | 浓硝酸使紫色石蕊试液先变红后褪色--酸性和强氧化性 | |
| B. | 不能用稀硝酸与锌反应制氢气--强氧化性 | |
| C. | 要用棕色瓶盛装浓硝酸--稳定性 | |
| D. | 能使滴有酚酞的氢氧化钠溶液红色褪去--强氧化性 |
2.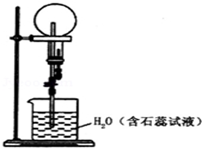 已知NH3和HCl都能用来作喷泉实验的气体,若在相同条件下用等体积烧瓶各收集满NH3和HCl气体,进行实验(两烧瓶内充满溶液且不考虑溶质的扩散).下列说法正确的是( )
已知NH3和HCl都能用来作喷泉实验的气体,若在相同条件下用等体积烧瓶各收集满NH3和HCl气体,进行实验(两烧瓶内充满溶液且不考虑溶质的扩散).下列说法正确的是( )
 已知NH3和HCl都能用来作喷泉实验的气体,若在相同条件下用等体积烧瓶各收集满NH3和HCl气体,进行实验(两烧瓶内充满溶液且不考虑溶质的扩散).下列说法正确的是( )
已知NH3和HCl都能用来作喷泉实验的气体,若在相同条件下用等体积烧瓶各收集满NH3和HCl气体,进行实验(两烧瓶内充满溶液且不考虑溶质的扩散).下列说法正确的是( )| A. | NH3和HCl分别形成红色、蓝色喷泉 | |
| B. | 制备干燥的NH3和HCl,可分别用无水CaCl2、碱石灰干燥 | |
| C. | 改为NO2气体,所得溶液溶质的物质的量浓度与前两者不同 | |
| D. | 去掉装置中的胶头滴管,改为单孔塞,也可引发喷泉 |
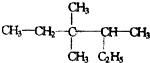 3,3,4-三甲基己烷
3,3,4-三甲基己烷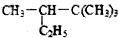 2,2,3-三甲基戊烷
2,2,3-三甲基戊烷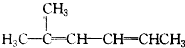 2-甲基-2,4-己二烯
2-甲基-2,4-己二烯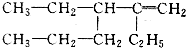 2,3-二乙基-1-己烯.
2,3-二乙基-1-己烯.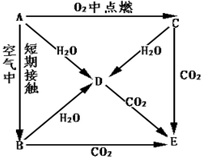 A、B、C、D、E五种物质的焰色反应均为黄色,且A为单质,它们按图所示关系相互转化.
A、B、C、D、E五种物质的焰色反应均为黄色,且A为单质,它们按图所示关系相互转化. 
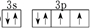
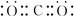
 ,该电子排布图错误的理由是违背了洪特规则.
,该电子排布图错误的理由是违背了洪特规则.