题目内容
16.下列反应的离子方程式不正确的是( )| A. | 氨气通入稀硫酸中:NH3+H+═NH4+ | |
| B. | 小苏打溶液和烧碱溶液反应:HCO3-+2OH-═CO32-+H2O | |
| C. | 一小块金属钠投入水中:Na+2H2O═Na++OH-+H2↑ | |
| D. | 澄清石灰水中加入过量硝酸:H++OH-═H2O |
分析 A.氨气与稀硫酸反应生成硫酸铵;
B.小苏打为碳酸氢钠,烧碱为氢氧化钠,碳酸氢钠和氢氧化钠按照物质的量1:1反应生成碳酸钠和水;
C.钠与水反应生成氢氧化钠,2mol钠生成1mol氢气,该离子方程式不满足电子守恒;
D.氢氧化钙与稀硝酸反应生成硝酸钙和水,澄清石灰水中的氢氧化钙需要拆开.
解答 解:A.氨气通入稀硫酸中,反应生成硫酸铵,反应的离子方程式为:NH3+H+═NH4+,故A正确;
B.小苏打溶液和烧碱溶液反应生成碳酸钠和水,氢氧根离子的系数应该为1,正确的离子方程式为:HCO3-+OH-═CO32-+H2O,故B错误;
C.一小块金属钠投入水中,反应生成氢氧化钠和氢气,正确的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,故C错误;
D.澄清石灰水中加入过量硝酸,反应生成硝酸钙和水,反应的离子方程式为:H++OH-═H2O,故D正确;
故选BC.
点评 本题考查了离子方程式的正误判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
相关题目
7.下列说法错误的是( )
| A. | 摘下几根火柴头,浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸,若出现白色沉淀,说明含氯元素 | |
| B. | 纸层析法分离叶绿素a和叶绿素b时,若点样的斑点太大,则会导致色谱分离不清 | |
| C. | 在抽滤装置中洗涤沉淀时,应关小水龙头,使洗涤剂缓慢通过沉淀物 | |
| D. | 在Zn-Cu原电池中加入高锰酸钾、双氧水等强氧化剂,灯泡亮度增加且持续时间较长 |
4.Al、Fe、Cu都是重要的金属元素.下列说法正确的是( )
| A. | 三种元素对应的氧化物均为碱性氧化物 | |
| B. | 三者的单质长期放置在空气中均能被腐蚀 | |
| C. | 制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 | |
| D. | 电解AlCl3、FeCl3、CuCl2的混合溶液时,阴极上依次析出Cu、Fe、Al |
1.下列离子方程式书写正确的是( )
| A. | 将金属钠投入水中:Na+2H2O═Na++OH-+H2↑ | |
| B. | 过量CO2通人Ca(ClO)2溶液中:ClO-+CO2+H2O═HCO3-+HCIO | |
| C. | NH4HCO3溶液与过量的NaOH溶液反应:NH4++OH-═NH3↑+H2O | |
| D. | 铜片溶于稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
8.下列叙述正确的是( )
| A. | Fe与S混合加热生成FeS2 | |
| B. | NaHCO3的热稳定性大于Na2CO3 | |
| C. | 白磷在空气中加热到一定温度能转化为红磷 | |
| D. | 过量的铜与稀硝酸反应有一氧化氮生成 |
6.2008年北京奥运会“祥云”火炬用的是环保型燃料--丙烷(C3H8),悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷,下列有关说法正确的是( )
| A. | 丙烷分子中三个碳原子在一条直线上 | |
| B. | 符合通式CnH2n+2的均属于烷烃 | |
| C. | 丙烷的二氯代物有5种 | |
| D. | 丁烷能与氯气在光照时发生加成反应 |
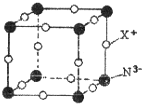 氮元素可形成卤化物、氮化物、叠氮化物及配合物等许多化合物.
氮元素可形成卤化物、氮化物、叠氮化物及配合物等许多化合物.