题目内容
6.某有机物A 3.0克,完全燃烧后生成3.6克水和3.36L二氧化碳(标准状况),已知该有机物的蒸汽对氢气的相对密度为30,求该有机物的分子式;若该有机物为醇类,写出其结构简式.分析 根据n=$\frac{m}{M}$、n=$\frac{V}{{V}_{m}}$计算出水、二氧化碳的物质的量,再根据m=nM计算出3.0g该有机物分子中含有的碳氢元素质量,从而确定该有机物分子中是否含有氧元素及含有氧元素的物质的量,据此计算出该有机物的最简式,再根据相对密度计算出该有机物的相对分子质量,据此确定该有机物的分子式;
该有机物为醇类,分子中含有羟基,根据分子式确定该有机物结构简式.
解答 解:3.6g水的物质的量为:$\frac{3.6g}{18g/mol}$=0.2mol,0.2mol水中含有0.4molH原子,含有H的质量为:1g/mol×0.4mol=0.4g,
标况下3.36L二氧化碳的物质的量为:$\frac{3.36L}{22.4L/mol}$=0.15mol,含有C的质量为:12g/mol×0.15mol=1.8g,
3.0g该有机物分子中含有碳氢的质量为:1.8g+0.4g=2.2g<3.0g,
说明该有机物分子中含有氧元素,含有氧元素的物质的量为:$\frac{3.0g-2.2g}{16g/mol}$=0.05mol,
该有机物分子中含有C、H、O的物质的量之比为:0.15mol:0.4mol:0.05mol=3:8:1,
该有机物最简式为:C3H8O,
该有机物的蒸汽对氢气的相对密度为30,则该有机物的相对分子质量为:30×2=60,
该有机物分子式为:C3H8O,
该有机物分子中含有羟基,试确定该有机物的结构简式有:1-丙醇:CH3-CH2-CH2-OH,2-丙醇: ,
,
答:该有机物分子式为C3H8O;该有机物的结构简式为CH3-CH2-CH2-OH、 .
.
点评 本题考查有机物分子式、结构简式的确定,题目难度中等,注意根据生成物的质量和有机物的质量判断有机物中是否含有O元素为解答该题的关键,注意质量守恒在化学计算中的应用方法.

 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案| A. | 硫酸工业中合成SO3通常采用常压,是因为常压比高压更有利于SO3的生成 | |
| B. | 氯碱工业中阳离子交换膜的主要作用是防止氯气和氢气以及氢氧化钠反应 | |
| C. | 工业合成氨通常采用500℃的高温主要是为了提高氮气的转化率 | |
| D. | 电解精炼铜时,纯铜作为阳极,粗铜作为阴极 |
| A. | 用水将苯、乙酸、四氯化碳区分开来 | |
| B. | 在实验室中通常将钠保存在汽油里 | |
| C. | 用稀硝酸洗去残留在试管壁上的银 | |
| D. | 如果苯酚溶液沾到皮肤上,应立即用酒精洗涤 |
| 配料 | 氯化钠(NaCl)、碘酸钾(KIO3) |
| 含碘量 | 20~40mg•kg-1 |
| 保质期 | 18个月 |
| 食用方法 | 勿长时间炖炒 |
| 贮藏指南 | 避热、避光、密封、防潮 |
(2)将5.0g该“加碘食盐”溶于水中配成100mL溶液,该溶液中IO${\;}_{3}^{-}$离子物质的量浓度为多少?
| A. | 氨气通入稀硫酸中:NH3+H+═NH4+ | |
| B. | 小苏打溶液和烧碱溶液反应:HCO3-+2OH-═CO32-+H2O | |
| C. | 一小块金属钠投入水中:Na+2H2O═Na++OH-+H2↑ | |
| D. | 澄清石灰水中加入过量硝酸:H++OH-═H2O |
 .
.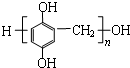 单体是
单体是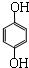 和HCHO,聚合物
和HCHO,聚合物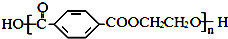 单体是HOCH2CH2OH、
单体是HOCH2CH2OH、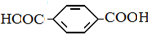
 ,基态原子核外电子排布式1s22s22p63s23p63d24s2.该元素的原子序数为22,该元素是金属元素(填“金属”或“非金属”).
,基态原子核外电子排布式1s22s22p63s23p63d24s2.该元素的原子序数为22,该元素是金属元素(填“金属”或“非金属”).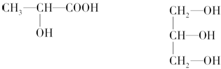
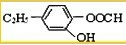
 ,它可以通过不同的反应得到下列物质:
,它可以通过不同的反应得到下列物质: C.
C. D.
D.
 .
. ;
; .
.