题目内容
1.下列关于乙醇和乙酸的说法错误的是( )| A. | 乙醇和乙酸都是常用调味品的主要成分 | |
| B. | 相同条件下,与金属钠反应的速率,乙醇比乙酸慢 | |
| C. | 乙醇可由乙烯与水发生加成反应制得,乙酸可由乙醇氧化制得 | |
| D. | 乙醇和乙酸之间能发生酯化反应,酯化反应的逆反应为皂化反应 |
分析 乙醇中含-OH、乙酸中含-COOH,均具有刺激性气味、均与Na反应,二者可发生酯化反应,而皂化反应为油脂在碱性溶液中的水解反应,以此来解答.
解答 解:A.乙醇和乙酸均具有刺激性气味,都是常用调味品的主要成分,故A正确;
B.相同条件下,与金属钠反应的速率,-COOH易电离出氢离子,则乙醇比乙酸慢,故B正确;
C.乙烯与水发生加成反应生成乙醇,乙醇被强氧化剂氧化制得乙酸,故C正确;
D.乙醇和乙酸之间能发生酯化反应,酯化反应为可逆反应,但油脂在碱性溶液中的水解反应为皂化反应,故D错误;
故选D.
点评 本题考查有机物的结构与性质,为高考常见题型和高频考点,侧重于学生的分析能力和应用能力的考查,注意把握官能团与性质的关系、有机反应,选项D中皂化反应为解答的易错点,题目难度不大.

练习册系列答案
相关题目
12.某无色溶液中,可以大量共存的离子组是( )
| A. | Cu2+、Na+、NO3-、Cl- | B. | NH4+、K+、HCO3-、OH- | ||
| C. | Na+、Al3+、AlO2-、Cl- | D. | K+、Mg2+、SO42-、HCO3- |
16.A、B、C、D均属于短周期元素.A是元素周期表所有元素中原子半径最小的;B和C都只有两个电子层,B中一层电子数是另一层的两倍;C中两层电子数之和是两层电子数之差的两倍;D中一层电子数是另两层电子数之和,下列说法中正确的是( )
| A. | C的简单离子还原性大于D | |
| B. | D元素只能以化合态存在于自然界中 | |
| C. | A元素所形成离子的半径有可能大于He原子的半径 | |
| D. | B、D的原子不能相互结合形成化合物 |
6.铅蓄电池在现代生活中有广泛应用,其电极材料是Pb和PbO2,电解液是硫酸溶液.现用铅蓄电池电解硫酸钠溶液一段时间后,假设电解时温度不变且惰性电极,下列说法正确的是( )
| A. | 蓄电池放电时,每消耗0.1molPb,共生成0.1mol PbSO4 | |
| B. | 电解硫酸钠溶液时的阳极反应式为:4OH--4e-=2H2O+O2↑ | |
| C. | 电解后,硫酸钠溶液中有晶体析出,但c(Na2SO4)会变小 | |
| D. | 蓄电池放电一段时间后其电解液中H2SO4的浓度、密度都变大 |
13.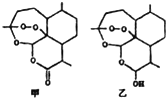 2015年我国药学家屠呦呦因创制青蒿素与双氢青蒿素用于治疗疟疾获得诺贝尔科学奖.图甲为青蒿素分子的结构简式,乙为双氢青蒿素分子的结构简式,其活性结构为分子中的“-O-O-”.下列说法错误的是( )
2015年我国药学家屠呦呦因创制青蒿素与双氢青蒿素用于治疗疟疾获得诺贝尔科学奖.图甲为青蒿素分子的结构简式,乙为双氢青蒿素分子的结构简式,其活性结构为分子中的“-O-O-”.下列说法错误的是( )
 2015年我国药学家屠呦呦因创制青蒿素与双氢青蒿素用于治疗疟疾获得诺贝尔科学奖.图甲为青蒿素分子的结构简式,乙为双氢青蒿素分子的结构简式,其活性结构为分子中的“-O-O-”.下列说法错误的是( )
2015年我国药学家屠呦呦因创制青蒿素与双氢青蒿素用于治疗疟疾获得诺贝尔科学奖.图甲为青蒿素分子的结构简式,乙为双氢青蒿素分子的结构简式,其活性结构为分子中的“-O-O-”.下列说法错误的是( )| A. | 甲分子式为C15H22O5 | |
| B. | 甲、乙分子中均只存在2个六元环 | |
| C. | 甲转化成乙后水溶性增强 | |
| D. | 甲、乙分子中的活性结构“-O-O-”具有强氧化性 |