题目内容
1.醇(C5H12O)发生下列反应时,所得产物数目最少(不考虑立体异构)的是( )| A. | 与浓氢溴酸卤代 | B. | 与浓硫酸共热消去 | ||
| C. | 铜催化下氧化 | D. | 与戊酸催化酯化 |
分析 戊基-C5H11可能的结构有:-CH2CH2CH2CH2CH3、-CH(CH3)CH2CH2CH3、-CH(CH2CH3)2、-CHCH(CH3)CH2CH3、-C(CH3)2CH2CH3、-C(CH3)CH(CH3)2、-CH2CH2CH(CH3)2、-CH2C(CH3)3,所以该有机物的可能结构有8种,
A.-OH被-Br取代,同分异构体数目相同;
B.醇发生消去反应生成烯烃,可认为烷烃对应的烯烃;
C.在一定条件下能发生催化氧化反应,说明连接-OH的C原子上有H原子;
D.C5H12O对应的醇有8种,而戊酸有4种,以此可确定同分异构体数目.
解答 解:戊基-C5H11可能的结构有:-CH2CH2CH2CH2CH3、-CH(CH3)CH2CH2CH3、-CH(CH2CH3)2、-CHCH(CH3)CH2CH3、-C(CH3)2CH2CH3、-C(CH3)CH(CH3)2、-CH2CH2CH(CH3)2、-CH2C(CH3)3,所以该有机物的可能结构有8种,
A.与浓氢溴酸卤代,-OH被-Br取代,同分异构体数目相同,为8种;
B.醇对应的烷烃可为CH3CH2CH2CH2CH3、CH3CH2CH(CH3)2、C(CH3)4,醇发生消去反应生成烯烃,可认为烷烃对应的烯烃,其中CH3CH2CH2CH2CH3对应的烯烃有2种,CH3CH2CH(CH3)2对应的烯烃有3种,C(CH3)4没有对应的烯烃,共5种;
C.在一定条件下能发生催化氧化反应,说明连接-OH的C原子上有H原子,对应烃基可为:-CH2CH2CH2CH2CH3、-CH(CH3)CH2CH2CH3、-CH(CH2CH3)2、-CHCH(CH3)CH2CH3、-CH2CH2CH(CH3)2、-CH2C(CH3)3,共6种;
D.C5H12O对应的醇有8种,而戊酸有4种,对应的产物有32种,
则最少的为5种,
故选B.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握物质的性质以及同分异构体的数目的判断,本题思维量较大,做题时注意体会,难度较大.

 阅读快车系列答案
阅读快车系列答案| Zn的质量 | H2SO4的浓度 | 收集20mL H2所需的时间 | |
| ① | 10g(锌粒) | 0.1mol/L | 153s |
| ② | 10g(锌粉) | 0.1mol/L | 125s |
| ③ | 10g(锌粉) | 0.2mol/L | 62s |
(2)写出该反应的离子方程式Zn+2H+═Zn2++H2↑,
(3)经过试验对比,同学们在①组试验的试管中,滴入几滴CuSO4溶液后,锌粒表面有紫红色物质生成,同时发现试管中产生气泡的速度明显加快,请你分析,产生这种现象加快反应速率的原因是因为发生了原电池反应.
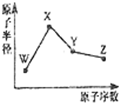 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差l;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.下列说法不正确的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差l;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.下列说法不正确的是( )| A. | 对应简单离子半径:W>X | |
| B. | 对应气态氢化物的稳定性:Y<Z | |
| C. | 化合物XZW既含离子键,又含极性共价键 | |
| D. | Z的氢化物和X的最高价氧化物对应水化物的溶液均能与Y的氧化物反应 |
| A. | 饱和NaHCO3溶液 | B. | Ca(HCO3)2溶液 | C. | Na2S溶液 | D. | AlCl3溶液 |
| A. | 氢氧化镁和稀盐酸反应 | B. | Ba(OH)2溶液滴入稀硫酸中 | ||
| C. | 二氧化碳通入澄清石灰水中 | D. | 澄清石灰水和稀硝酸反应 |
| A. | 一定大于92.0 kJ | B. | 一定等于92.0 kJ | C. | 一定小于92.0 kJ | D. | 不能确定 |

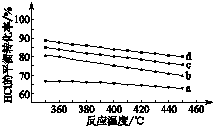 用Cl2生产含氯有机物时会产生HCl.利用反应4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)可实现氯的循环利用.
用Cl2生产含氯有机物时会产生HCl.利用反应4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)可实现氯的循环利用.