题目内容
11.某实验小组进行了“影响化学反应速率”的探究实验,原始数据记录如下:| Zn的质量 | H2SO4的浓度 | 收集20mL H2所需的时间 | |
| ① | 10g(锌粒) | 0.1mol/L | 153s |
| ② | 10g(锌粉) | 0.1mol/L | 125s |
| ③ | 10g(锌粉) | 0.2mol/L | 62s |
(2)写出该反应的离子方程式Zn+2H+═Zn2++H2↑,
(3)经过试验对比,同学们在①组试验的试管中,滴入几滴CuSO4溶液后,锌粒表面有紫红色物质生成,同时发现试管中产生气泡的速度明显加快,请你分析,产生这种现象加快反应速率的原因是因为发生了原电池反应.
分析 (1)实验②与③中锌的表面积相同,硫酸浓度大的反应速率更快;实验①与②硫酸的浓度相同,表面积大的锌粉反应速率更快;
(2)锌与硫酸反应生成硫酸锌和氢气;
(3)锌与铜离子反应生成铜单质,形成铜、锌、稀硫酸原电池,原电池加快反应速率.
解答 解:(1)实验②与③中锌的表面积相同,硫酸浓度大的反应速率更快,收集20mLH2所需的时间更短,则H2SO4的浓度增加,反应速率加快,实验①与②硫酸的浓度相同,表面积大的锌粉反应速率更快,收集20mLH2所需的时间更短,则实验①与②比较的是固体接触面积对反应速率的影响,
故答案为:H2SO4;加快;固体接触面积;
(2)锌与硫酸反应生成硫酸锌和氢气,反应离子方程式为:Zn+2H+=Zn2++H2↑,
故答案为:Zn+2H+=Zn2++H2↑;
(3)在①组试验的试管中,滴入几滴CuSO4溶液,锌与铜离子反应生成铜单质,形成铜、锌、稀硫酸原电池,原电池加快反应速率,
故答案为:原电池反应.
点评 本题考查了影响化学反应速率的因素,浓度、接触面积不同反应速率不同,掌握基础是解题关键,注意对比实验中控制变量的分析方法,题目比较简单.

练习册系列答案
相关题目
10.下列有关钠及其化合物的说法不正确的是( )
| A. | 电解饱和食盐水不可制取金属钠 | |
| B. | 钠与氧气反应的产物与反应条件有关 | |
| C. | 过氧化钠与水反应不能生成氢氧化钠 | |
| D. | 钠可以从四氯化钛中置换出钛 |
11.美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示).下列有关该工艺的说法错误的是( 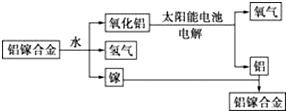 )
)
 )
)| A. | 该过程中,能量的转化形式只有两种 | |
| B. | 铝镓合金可以循环使用 | |
| C. | 铝镓合金与水反应的化学方程式为2Al+3H2O═Al2O3+3H2↑ | |
| D. | 总反应式为2H2O═2H2↑+O2↑ |
6.小明体检的血液化验单中,葡萄糖为5.9mmol/L.该体检指标的物理量是( )
| A. | 物质的量浓度 | B. | 溶解度 | C. | 质量分数 | D. | 摩尔质量 |
16.甲~辛等元素在周期表中的位置如表所示.下列说法不正确的是( )
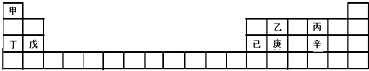

| A. | 甲、丁、戊的单质都是金属 | |
| B. | 乙、丙、辛都是非金属元素 | |
| C. | 乙、庚、辛都能形成氧化物 | |
| D. | 已的氧化物既可溶于KOH溶液又可溶于H2SO4溶液 |
20.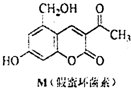 天然化合物M(假蜜环菌素)的结构简式如图所式.对M的结构与性质叙述错误的是( )
天然化合物M(假蜜环菌素)的结构简式如图所式.对M的结构与性质叙述错误的是( )
 天然化合物M(假蜜环菌素)的结构简式如图所式.对M的结构与性质叙述错误的是( )
天然化合物M(假蜜环菌素)的结构简式如图所式.对M的结构与性质叙述错误的是( )| A. | M的分子式为C12H10O5 | |
| B. | M能发生取代反应、加成反应、氧化反应、还原反应 | |
| C. | M中碳原子之间全部以C-C键或C=C键相互结合 | |
| D. | M的同分异构体最多含有2个与乙酸相同的官能团 |
1.醇(C5H12O)发生下列反应时,所得产物数目最少(不考虑立体异构)的是( )
| A. | 与浓氢溴酸卤代 | B. | 与浓硫酸共热消去 | ||
| C. | 铜催化下氧化 | D. | 与戊酸催化酯化 |

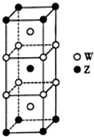 短周期元素T、X、Y、Z的原子序数依次增大,其中元素T、X基态原子均有2个未成对电子,元素Y基态原子s能级的电子总数与p能级的电子总数相等,元素Z的价电子数等于能层数.元素W位于第四周期,其基态原子所含未成对电子数在该周期中最多.
短周期元素T、X、Y、Z的原子序数依次增大,其中元素T、X基态原子均有2个未成对电子,元素Y基态原子s能级的电子总数与p能级的电子总数相等,元素Z的价电子数等于能层数.元素W位于第四周期,其基态原子所含未成对电子数在该周期中最多.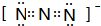 .
.