题目内容
9.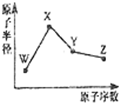 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差l;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.下列说法不正确的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差l;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.下列说法不正确的是( )| A. | 对应简单离子半径:W>X | |
| B. | 对应气态氢化物的稳定性:Y<Z | |
| C. | 化合物XZW既含离子键,又含极性共价键 | |
| D. | Z的氢化物和X的最高价氧化物对应水化物的溶液均能与Y的氧化物反应 |
分析 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.Y的单质是一种常见的半导体材料,则Y为Si;已知W的一种核素的质量数为18,中子数为10,则W的质子数为8,W为O;由原子序数可知,X、Y、Z均为第三周期元素,X和Ne原子的核外电子数相差l,X为Na;Z的非金属性在同周期元素中最强,则Z为Cl,然后结合元素周期律及元素化合物知识来解答.
解答 解:W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.Y的单质是一种常见的半导体材料,则Y为Si;已知W的一种核素的质量数为18,中子数为10,则W的质子数为8,W为O;由原子序数可知,X、Z均为第三周期元素,X和Ne原子的核外电子数相差l,X为Na;Z的非金属性在同周期元素中最强,则Z为Cl,
A.具有相同电子排布的离子,原子序数大的离子半径小,则对应简单离子半径:W>X,故A正确;
B.非金属性越强,对应氢化物越稳定,则对应气态氢化物的稳定性:Y<Z,故B正确;
C.化合物XZW为NaClO,既含离子键,又含极性共价键,故C正确;
D.Z的氢化物为HCl,X的最高价氧化物对应水化物的溶液为NaOH溶液,只有NaOH能与Y的氧化物(二氧化硅)反应,而盐酸与二氧化硅不反应,故D错误;
故选D.
点评 本题考查原子结构与元素周期律等,为高频考点,把握元素的位置、元素的性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意周期律及元素化合物知识的应用,题目难度不大.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
20.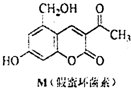 天然化合物M(假蜜环菌素)的结构简式如图所式.对M的结构与性质叙述错误的是( )
天然化合物M(假蜜环菌素)的结构简式如图所式.对M的结构与性质叙述错误的是( )
 天然化合物M(假蜜环菌素)的结构简式如图所式.对M的结构与性质叙述错误的是( )
天然化合物M(假蜜环菌素)的结构简式如图所式.对M的结构与性质叙述错误的是( )| A. | M的分子式为C12H10O5 | |
| B. | M能发生取代反应、加成反应、氧化反应、还原反应 | |
| C. | M中碳原子之间全部以C-C键或C=C键相互结合 | |
| D. | M的同分异构体最多含有2个与乙酸相同的官能团 |
17.下列离子方程式正确的是( )
| A. | 往碳酸镁中滴加稀盐酸:CO32-+2H+═CO2↑+H2O | |
| B. | 浓烧碱溶液中加入铝片:Al+2OH-═AlO2-+H2↑ | |
| C. | 氯化钙与碳酸氢钾溶液混合:Ca2++CO32-═CaCO3↓ | |
| D. | 用惰性电极电解氯化镁溶液:Mg2++2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+Mg(OH)2↓ |
4.下列各溶液中,微粒的物质的量浓度关系表述正确的是( )
| A. | 0.1 mol/LNa2CO3溶液中:c(Na+)═(HCO3-)+c(H2CO3)+2c(CO32-) | |
| B. | pH=l2的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)相等 | |
| C. | 将0.2mol/LNaA溶液和0.1 mol•L-1盐酸溶液等体积混合所得碱性溶液中:c(Na+)+c(H+)═c(A-)+c(Cl-) | |
| D. | 常温下pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7 |
14.有关晶体与导电性的关系叙述正确的是( )
| A. | 水溶液导电的一定是分子晶体 | B. | 熔融态导电的一定是离子晶体 | ||
| C. | 原子晶体固态一定不导电 | D. | 分子晶体熔融态一定不导电 |
1.醇(C5H12O)发生下列反应时,所得产物数目最少(不考虑立体异构)的是( )
| A. | 与浓氢溴酸卤代 | B. | 与浓硫酸共热消去 | ||
| C. | 铜催化下氧化 | D. | 与戊酸催化酯化 |
18.短周期主族元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是次外层的2倍,Y的氟化物YF3分子中各原子均达到8电子稳定结构,Z是同周期中原子半径最大的元素,W的最高正价为+7价.下列说法不正确的是( )
| A. | X元素可以组成多种单质 | |
| B. | Y和Z可能在同一周期 | |
| C. | X与W形成的化合物和Z与W形成的化合物的化学键类型不同 | |
| D. | 元素X、Y、W的最高价氧化物对应水化物的酸性强弱:X<Y<W |
19.为解决全球能源与环境问题,节能减排已成共识.下列措施有利于节能减排的有( )
| A. | 举行“地球一小时”熄灯活动 | B. | 露天焚烧稻草和秸秆 | ||
| C. | 夏天将空调的温度设置在26℃以上 | D. | 生活垃圾分类回收处理 |
