题目内容
18.草酸二酯是荧光棒产生荧光现象的主要物质,其结构简式如图所示.下列有关说法正确的是( )
| A. | 草酸二酯的分子中所有碳原子一定共平面 | |
| B. | 草酸二酯水解后生成醇的分子式为C5H12O | |
| C. | 草酸二酯中苯环上氢原子被一个溴原子取代的有机产物有两种 | |
| D. | 1 mol草酸二酯与足量NaOH溶液反应最多消耗4 mol NaOH |
分析 由结构可知,该物质为大分子,含苯环、-COOC-、-Cl,结合酯、卤代烃的性质来解答.
解答 解:A.含有饱和碳原子,具有甲烷的结构特点,则所有的碳原子不能共平面,故A错误;
B.含有两个酯基,水解生成的醇含有5个C,为C5H12O,故B正确;
C.草酸二酯每个苯环上只含有1个H,且结构对称,则草酸二酯苯环上氢原子被一个溴原子取代的产物只有一种,故C错误;
D.-COOC-与碱反应,且水解生成的苯酚结构也与NaOH溶液反应,则1mol草酸二酯与氢氧化钠稀溶液反应(苯环上卤素不水解),最多消耗6molNaOH,故D错误.
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物结构及对称性为解答的关键,侧重分析与迁移应用能力的考查,题目难度不大.

练习册系列答案
相关题目
9.25℃时,向盛有50mL pH=2的一元酸HA溶液的绝热容器中加入pH=13的NaOH溶液,加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如图所示.下列叙述正确的是( )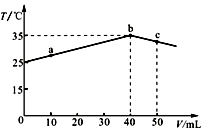

| A. | a→b的过程中,溶液中c(A-)与c(HA)之和始终不变 | |
| B. | b点表示酸碱恰好完全反应 | |
| C. | 等浓度的NaOH和NaA混合溶液中一定存在关系:c(Na+)>c(A-)>c(H+)>c(OH-) | |
| D. | 25℃时,HA的电离平衡常数Ka约为1.23×10-3 |
13.设NA为阿伏加德罗常数值,下列有关叙述正确的是( )
| A. | 标准状况下,11.2L CH2C12含极性共价键数目为2NA | |
| B. | 含1 mol Cl-的NH4Cl溶液中加入适量氨水使溶液呈中性,此时溶液中NH4+的数目大于NA | |
| C. | 4.6g甲苯(C7H8)和丙三醇(C3H8O3)混合物中含H原子数目为0.4NA | |
| D. | 将1mol Cl2通入足量水中,溶液中HC1O、Cl-、ClO-粒子数之和为2NA |
3.已知咖啡酸的结构如图所示.关于咖啡酸的描述正确的是( )
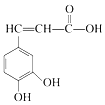

| A. | 与咖啡酸的物质类别完全相同(含咖啡酸),且苯环上只有3个取代基的同分异构体(包括顺反异构)有18种 | |
| B. | 1mol咖啡酸最多可与3molBr2反应 | |
| C. | 咖啡酸与 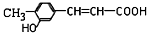 互为同系物 互为同系物 | |
| D. | 1mol咖啡酸与足量NaHCO3溶液反应产生3mol气体 |
10.下列离子方程式正确的是( )
| A. | 氯气和水反应:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 金属钠投入MgCl2溶液中:2Na+Mg2+═2Na++Mg | |
| C. | 0.1mol/LNaHSO4溶液与0.1mol/LBa(OH)2溶液等体积混合:SO42-+Ba2+=BaSO4↓ | |
| D. | 硅酸钠水溶液中通入过量CO2:SiO32-+2H2O+2CO2═2HCO3-+H2SiO3↓ |
7.能用于鉴别CO2 和SO2 的试剂是( )
| A. | 硝酸钡溶液 | B. | 澄清石灰水 | C. | 紫色石蕊试液 | D. | 氯化钡溶液 |
12.检验SO42-离子,除了需要用到BaCl2,还要用到的试剂是( )
| A. | HNO3 | B. | AgNO3 | C. | HCl | D. | H2SO4 |
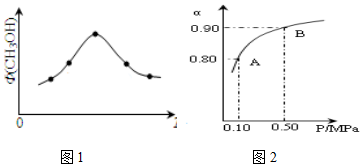 科学家为实现“低碳”构想,把空气中的CO2转化为可再生能源甲醇(CH3OH).该反应的热化学方程式为:
科学家为实现“低碳”构想,把空气中的CO2转化为可再生能源甲醇(CH3OH).该反应的热化学方程式为: