��Ŀ����
14��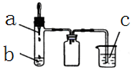 ������ͼ��ʾװ�ý�������ʵ�飬ʵ����������۾���ȷ���ǣ�������
������ͼ��ʾװ�ý�������ʵ�飬ʵ����������۾���ȷ���ǣ�������| ѡ�� | ʵ���Լ� | ʵ������ | ʵ����� | ||
| a | b | c | |||
| A | Ũ��ˮ | ��ʯ�� | FeCl2��Һ | ������ɫ������Ѹ�ٱ�Ϊ����ɫ������Ϊ���ɫ | �������������� |
| B | ϡ���� | FeS | AgCl����Һ | ����Һ�ɰ�ɫ��Ϊ��ɫ | Ksp��AgCl����Ksp��Ag2S�� |
| C | Ũ���� | ͭ | BaSO3����Һ | ����Һ����� | +4������л�ԭ�� |
| D | Ũ���� | KMnO4 | ��ɫʯ����Һ | ��Һ�ȱ�����ɫ | Cl2�����Ժ�Ư���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� A��Ũ��ˮ���ʯ�һ�ϵõ�������������c���Ȼ�������Һ��Ӧ�������������������������������ٱ�����������������������
B��ϡ������FeS��Ӧ�������⣬��c����AgCl����������ת����
C��Cu��Ũ���ᷴӦ���ɶ������������������������ᱵ����������ԭ��Ӧ��
D��Ũ�����������ط�������ԭ��Ӧ����������������ˮ��Ӧ���������HClO���Դ������
��� �⣺A��Ũ��ˮ���ʯ�һ�ϵõ�������������c���Ȼ�������Һ��Ӧ�������������������������������ٱ������������������������������ɫ������Ѹ�ٱ�Ϊ����ɫ������Ϊ���ɫ������ʵ�鲻��˵���������������ԣ���A����
B��ϡ������FeS��Ӧ�������⣬��c����AgCl����������ת����������Һ�ɰ�ɫ��Ϊ��ɫ����֪Ksp��AgCl����Ksp��Ag2S������B��ȷ��
C��Cu��Ũ���ᷴӦ���ɶ������������������������ᱵ����������ԭ��Ӧ����c�а�ɫ��������ʧ�������������ɣ���C����
D��Ũ�����������ط�������ԭ��Ӧ����������������ˮ��Ӧ���������HClO������Һ�ȱ�����ɫ�����������������Ժ�Ư���ԣ���D����
��ѡB��
���� ���⿼�黯ѧʵ�鷽�������ۣ�Ϊ��Ƶ���㣬�������ʵ����ʼ������ķ�Ӧ������ת����Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע�⻯ѧ��Ӧԭ����ʵ��װ�õ����ã���Ŀ�ѶȲ���

 �������������ɫ�ͳ����µ�Ksp���±���ʾ��
�������������ɫ�ͳ����µ�Ksp���±���ʾ��| Cu��OH��2 | CuOH | CuCl | Cu2O | |
| ��ɫ | ��ɫ | ��ɫ | ��ɫ | ש��ɫ |
| Ksp��25�棩 | 1.6��10-19 | 1.0��10-14 | 1.2��10-6 | - |
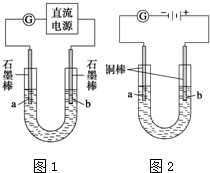
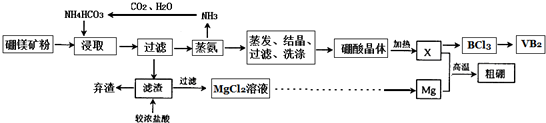
ʵ���װ����ͼ1��ʾ����ͨ��Դ����a��b�缫�Ͼ������ݲ�����
��1���������е������ӷ�Ӧ����ʽΪ2Cl-+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2OH-+H2��+Cl2����
��2��Ϊ��ȷ����Դ���������������в���һ����֮��Ч����BD��
A���۲����������������ɫ
B����U�ι����˷ֱ�������η�̪��Һ
C����ȼ�ŵ�ľ������U�ιܿ�
D����U�ιܿ���һ��ʪ��ĵ���KI��ֽ
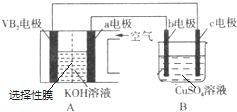
ʵ�����������װ�õ�ʯī������ͭ������ֱ����Դ���е�⣬װ����ͼ2��ʾ��
�۲쵽������������ʾ��
�ٿ�ʼ�������������Һ�����µ�ͭ�������䰵��
��5min��b��������ʼ���ְ�ɫ�������������࣬����a����ɢ��
��10min�����a���İ�ɫ������ʼ��ɺ�ɫ��
��12min��b�������İ�ɫ������ʼ��ɻ�ɫ��Ȼ����ɳȻ�ɫ��
��a��һֱ�д������ݲ�����
��ֹͣ��⣬��U�ι�������Һ����һ��ʱ����ϲ���Һ����ɫ��û�г�����ɫ���²����ȫ����ש��ɫ��
��3��a�������ĵ缫��Ӧ����ʽΪ2H++2e-=H2������2H2O+2e-�T2OH-+H2������
��4�����5min��b�������ĵ缫��Ӧ����ʽΪCu+Cl--e-�TCuCl����
��5��12min��b���������ֵijȻ�ɫ�����ijɷ���CuOH��Cu2O��ԭ����Ksp��CuOH����Ksp��CuCl����CuClת��Ϊ��ɫ��CuOH������CuOH���ȶ��ֽ�����Cu2O�����ԳȻ�ɫ�����ijɷ�ΪCuOH��Cu2O�Ļ���
| A�� | ����������ˮ������ˮ�м�����������ʹ��ˮ���� | |
| B�� | ���ӽ���Ĥ�ڹ�ҵ��Ӧ�ù㷺�����ȼҵ��ʹ�������ӽ���Ĥ | |
| C�� | ������һ�������Խ�ǿ�����壬����������ˮ������ | |
| D�� | SO2���л�ԭ�ԣ�������֪Ũ�ȵ�KMnO4��Һ�ⶨʳƷ��SO2������ |
 ���ȱ�������һ��ҩ���м��壬���ö��ȼױ�Ϊԭ�ϣ�ͨ����������������Ʊ�����Ӧ���£�
���ȱ�������һ��ҩ���м��壬���ö��ȼױ�Ϊԭ�ϣ�ͨ����������������Ʊ�����Ӧ���£���
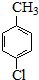 $��_{����}^{KMnO_{4}}$
$��_{����}^{KMnO_{4}}$
��
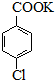 $\stackrel{H+}{��}$
$\stackrel{H+}{��}$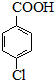
�йػ�����������������±���
| �۵�/�� | �е�/�� | �ܶ�/g•cm��3 | ��ɫ | ˮ���� | |
| ���ȼױ� | 7.5 | 162 | 1.07 | ��ɫ | ���� |
| ���ȱ����� | 243 | 275 | 1.54 | ��ɫ | �� |
| ���ȱ������ | �����ε�ͨ�ԣ����ڿ������Σ��ܽ�����¶����߶����� | ||||
���ڹ��Ϊ250mL��������ƿ��װ��A���м���һ�����Ĵ���������KMnO4��100mLˮ��
����ͼ��װ��װ�ã��ڷ�Һ©����װ��C���м���6.00mL���ȼױ���������93��ʱ����ε�����ȼױ���
�ۿ����¶���93�����ң���Ӧ2h���ˣ�ϴ����������ϴ��Һ����Һ�ϲ�������ϡ�����ữ��
�ܼ���Ũ������ȴ�ᾧ�����ˣ�ϴ����������������������Ϊwg��
��ش��������⣺
��1��װ��B�������������ܣ�
��2�������й�ʵ���˵������ȷ����AB
A����ȡ6.00mL���ȼױ���ѡ��25mL��ʽ�ζ���
B��װ��B��ˮ������ɴ�b�ڽ�a�ڳ�
C�������¶���93�����ң���ò���ˮԡ����
D��ȡ��������һ��ϴ��Һ�������Թ��У������е���BaCl2��Һ���ɼ��������Ƿ�ϴ�Ӹɾ�
��3��������ж��ȼױ��ļ��뷽������μ��������һ���Լ��룬�����Ǽ��ٶ��ȼױ��Ļӷ������ԭ�������ʣ�
��4��������й��˵�Ŀ���dz�ȥMnO2����Һ�м���ϡ�����ữ���ɹ۲쵽��ʵ�������Dz�����ɫ������
��5��ϴ����������ʵ�ϴ�Ӽ����������C���������B��
A���Ҵ� B����ˮ C����ˮ D����Һ
��6������M1��ʾ���ȼױ���ʽ����M2��ʾ���ȱ������ʽ������ʵ����ʵļ������ʽΪ$\frac{w}{\frac{6��1.07{M}_{2}}{{M}_{1}}}$��100%����Ҫ����㣩��
| A�� | �����ʵ������������������ֱ���ȫȼ�գ����߷ų������� | |
| B�� | ��H+��aq��+OH-��aq��=H2O��l����H=-57.3kJ•mol-1��֪��������1 mol CH3COOH��ϡ��Һ�뺬1 mol NaOH��ϡ��Һ��ϣ��ų�������С��57.3kJ | |
| C�� | 300�桢30MPa�£���0.5molN2��g����1.5mol H2��g�������ܱ������г�ַ�Ӧ����NH3��g��������19.3kJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��?2NH3��g����H=-38.6kJ•mol-1 | |
| D�� | ��C��ʯī��=C�����ʯ����H=+1.90 kJ•mol-1��֪�����ʯ��ʯī�ȶ� |

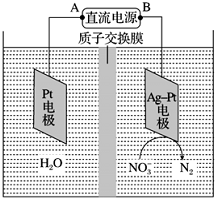 �绯ѧ����NO3-��ԭ����ͼ��ʾ��
�绯ѧ����NO3-��ԭ����ͼ��ʾ��