题目内容
18.下列各组物质中,分子数相同的一组是( )| A. | 2LCO和2LCO2 | B. | 标准状况下22.4LH2O和1mol O2 | ||
| C. | 0,4克H2和4.48L HCl | D. | 18克水和标准状况下22.4L CO2 |
分析 在标准状况下,气体的Vm=22.4L/mol,根据气体含有的分子数N=nNA=$\frac{m}{M}$NA=$\frac{V}{Vm}$NA来计算.
解答 解:A、相同条件下,相同体积的任何气体才具有相同的分子数,故A错误;
B、标准状况下1molO2的分子数为NA,22.4LH2O的分子数不是NA,因为标况下的水不是气态,故B错误;
C、0.4g氢气物质的量是0.2mol,H2的分子数为0.2NA,4.48LHCl气体在标况下的分子数才是0.2NA,题干没指名状态,所以4.48LHCl气体的分子数不一定是0.2NA,故C错误.
D、18gH2O的分子数N=$\frac{m}{M}$NA=$\frac{18g}{18g/mol}$NA=NA,标准状况下22.4LCO2的分子数N=$\frac{V}{Vm}$NA=$\frac{22.4L}{22.4L/mol}$NA=NA,即18gH2O和标准状况下22.4LCO2中分子数相同,故D正确;
故选D.
点评 本题考查学生有关物质的量和阿伏伽德罗常数的相关计算,可以根据所学知识来回答,难度不大.

练习册系列答案
相关题目
13.砷是氮族元素,黄砷(As4)是其一种单质,其分子结构与白磷(P4)相似,以下关于黄砷与白磷的比较叙述正确的是( )
| A. | 黄砷的熔点高于白磷 | B. | 黄砷中共价键键能大于白磷 | ||
| C. | 黄砷分子极性大于白磷 | D. | 分子中共价键键角均为109°28′ |
3.常温下,下面物质可用铁制或铝制容器盛放的是( )
| A. | 浓盐酸 | B. | 硫酸铜溶液 | C. | 稀硫酸 | D. | 浓硫酸 |
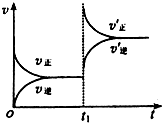 一定条件下2L的密闭容器中,反应aA(g)+bB(g)?cC(g)+dD(g)达到平衡.
一定条件下2L的密闭容器中,反应aA(g)+bB(g)?cC(g)+dD(g)达到平衡. 698K时,向某V L的密闭容器中充入2mol H2(g)和2mol I2(g),发生反应:H2(g)+I2(g)=2HI(g)△H=-26.5kJ•mol-1,测得各物质的物质的量浓度与时间变化的关系如图所示.
698K时,向某V L的密闭容器中充入2mol H2(g)和2mol I2(g),发生反应:H2(g)+I2(g)=2HI(g)△H=-26.5kJ•mol-1,测得各物质的物质的量浓度与时间变化的关系如图所示.