题目内容
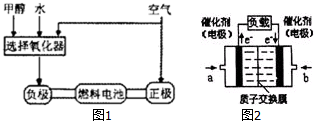
6.某同学用如图1所示装置制取氯水并进行相关实验.
(1)装置②中反应的化学方程式是Cl2+2NaOH=NaCl+NaClO+H2O;
(2)取少量装置①中的溶液滴在蓝色石蕊试纸上,试纸先变红后褪色,说明氯水具有的性质是酸性和漂白性;
(3)①实验室常用NaOH溶液吸收多余的氯气,下列试剂也可用于吸收氯气的是bc(填字母);
a.NaCl溶液 b.FeSO4溶液 c.Na2SO3溶液
②写出①中你选择的吸收试剂与Cl2反应的离子方程式:2Fe2++Cl2=2Fe3++2Cl-,H2O+SO32-+Cl2=SO42-+2Cl-+2H+;
(4)欲验证Cl2的氧化性强于I2,取少量装置①中的溶液加入盛有KI(填“KI”或“KIO3”)溶液的试管中,用力振荡后加入少量四氯化碳,振荡、静置,观察到的现象是液体分层、下层液体紫红色、上层液体无色.
(5)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生.某品牌消毒液包装上说明如图2.
①分析“对金属制品有腐蚀作用”的原因NaClO有强氧化性,而一般金属具有较强还原性;
②需“密闭保存”的原因消毒液的有效成分NaClO能与空气中的CO2作用,使其变质;
③“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式:Cl-+ClO-+2H+=Cl2↑+H2O.
分析 (1)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
(2)蓝色石蕊遇酸变红色,次氯酸具有漂白性;
(3)①氯气能够与碱反应,具有氧化性,能够与还原性物质发生反应据此解答;
②氯气与亚硫酸钠反应生成硫酸钠和氯化氢;
(4)元素的非金属性越强,其单质的氧化性越强,根据非金属单质之间的置换反应确定非金属性强弱,碘不易溶于水,易溶于有机溶剂;
(5)①次氯酸钠具有强的氧化性,能够氧化铁生成三价铁离子;
②消毒液有效成分是次氯酸盐与二氧化碳和水生成的次氯酸,次氯酸不稳定,见光分解;
③次氯酸根离子与氯离子发生氧化还原反应生成氯气和水.
解答 解:(1)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应方程式为Cl2+2NaOH=NaCl+NaClO+H2O,故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;
(2)蓝色石蕊遇酸变红色,次氯酸具有漂白性,取少量装置①中的溶液滴在蓝色石蕊试纸上,试纸先变红后褪色,说明氯水具有酸性和漂白性,故答案为:酸性和漂白性;
(3)①氯气能够与碱反应,具有氧化性,能够与还原性物质发生反应,可以用碱性物质或者还原性物质吸收,
a、氯化钠溶液不与氯气反应,故a错误;
b、氯气能够与硫酸亚铁反应,故b正确;
C、SO32-具有还原性,能够与氯气反应,可以吸收氯气,故 c正确;
故选:bc;
②亚铁离子与氯气反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,氯气与亚硫酸钠溶液反应的离子方程式:H2O+SO32-+Cl2=SO42-+2Cl-+2H+
故答案为:2Fe2++Cl2=2Fe3++2Cl-,H2O+SO32-+Cl2=SO42-+2Cl-+2H+;
(4)元素的非金属性越强,其单质的氧化性越强,氯气能氧化可溶性溴化物,装置①中的溶液加入KI,发生的离子反应为Cl2+2I-=I2+2Cl-,反应后的试管中,用力振荡后加入少量四氯化碳,振荡、静置,观察到的现象是液体分层、下层液体紫红色、上层液体无色,故答案为:KI;液体分层、下层液体紫红色、上层液体无色;
(5)①NaClO具有漂白作用,利用了NaClO的氧化性,而金属具有还原性,发生了氧化还原反应,对金属腐蚀,
故答案为:NaClO有强氧化性,而一般金属具有较强还原性;
②消毒液有效成分是次氯酸盐与二氧化碳和水生成的次氯酸,次氯酸不稳定,见光分解,所以应该密封保存;
故答案为:消毒液的有效成分NaClO能与空气中的CO2作用,使其变质;
③次氯酸根离子与氯离子发生氧化还原反应生成氯气和水,离子方程式:Cl-+ClO-+2H+=Cl2↑+H2O;
故答案为:Cl-+ClO-+2H+=Cl2↑+H2O.
点评 本题考查了氯气的性质和有关氧化还原反应、离子方程式的书写,题目难度中等,熟悉物质性质和相关规律是解题关键.

| A. | 3.2 g | B. | 4.8 g | C. | 5.4 g | D. | 3.8 g |
| A. | 燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 | |
| B. | 小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 | |
| C. | 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶 | |
| D. | 可用漂白粉和漂白液对地震后的受灾地区进行杀菌消毒 |
 反应A,可实现氯的循环利用。
反应A,可实现氯的循环利用。 4mol HCl被氧化,放出115.6kJ的热量。
4mol HCl被氧化,放出115.6kJ的热量。
 (一)发生在天津港“8•12”特大火灾爆炸事故,再一次引发了人们对环境问题的关注.
(一)发生在天津港“8•12”特大火灾爆炸事故,再一次引发了人们对环境问题的关注.