题目内容
18.某有机化合物,只含碳、氢、氧三种元素中的两种或三种,相对分子质量为74,完全燃烧时产生等物质的量的CO2和H2O.它的分子式可能为( )| A. | C4H10O | B. | C4H4O2 | C. | C3H6O2 | D. | C4H8O2 |
分析 该有机物完全燃烧时产生等物质的量的CO2和H2O,则该有机物分子中一定满足CnH2nOx(x可能为0),据此可排除A、B,然后根据C、D中有机物的相对分子质量判断.
解答 解:某有机化合物,只含碳、氢、氧三种元素中的两种或三种,相对分子质量为74,完全燃烧时产生等物质的量的CO2和H2O,则该有机物分子式一定满足:CnH2nOx(x可能为0),故A、B错误;
C.C3H6O2的相对分子质量为74,且满足CnH2nOx,故C正确;
D.C4H8O2的相对分子质量为88,不是74,故D错误;
故选C.
点评 本题考查了有机物分子式确定的计算,题目难度不大,注意掌握常见有机物组成、结构与性质,明确排除法在解答选择题中的应用方法,试题侧重基础知识的考查,培养了学生的分析能力及化学计算能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.检验Fe3+,最好的方法是加入( )
| A. | 氯水 | B. | KSCN溶液 | C. | 石蕊溶液 | D. | 酚酞溶液 |
6.试管内壁附着的以下物质用KOH溶液(必要时可加热)难以洗去的是( )
| A. | 硫 | B. | 油渍 | C. | 石炭酸 | D. | 酚醛树脂 |
6.已知:C(s)+O2(g)=CO2(g)△H1
CO2(g)+C(s)=2CO(g)△H2
2CO(g)+O2(g)=2CO2(g)△H3
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H4
下列关于上述反应焓变的判断正确的是( )
CO2(g)+C(s)=2CO(g)△H2
2CO(g)+O2(g)=2CO2(g)△H3
3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)△H4
下列关于上述反应焓变的判断正确的是( )
| A. | △H1>0 | B. | △H2<0 | C. | △H3<0 | D. | △H4<0 |
13.关于下列各装置图的叙述中,正确的是( )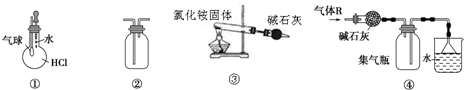

| A. | 装置①可验证HCl气体在水中的溶解性 | |
| B. | 装置②可用排空气法收集H2、NH3、Cl2、HCl、CO2等气体 | |
| C. | 装置③实验室用氯化铵制少量氨气 | |
| D. | 装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢 |
3.根据碘与氢气反应的热化学方程式(碘为气态或固态),下列判断正确的是( )
(ⅰ) I2(?)+H2(g)?2HI(g)△H=-9.48kJ/mol
(ⅱ) I2(?)+H2(g)?2HI(g)△H=26.48kJ/mol.
(ⅰ) I2(?)+H2(g)?2HI(g)△H=-9.48kJ/mol
(ⅱ) I2(?)+H2(g)?2HI(g)△H=26.48kJ/mol.
| A. | ⅰ中碘为气态,ⅱ中碘为固态 | |
| B. | 反应(ⅰ)的产物比反应(ⅱ)的产物稳定 | |
| C. | 1 mol I2(g)中通入1 mol H2(g),反应放热9.48 kJ | |
| D. | 1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
10.已知铅蓄电池放电时的反应为PbO2+2H2SO4+Pb═2PbSO4+2H2O.某兴趣小组用铅蓄电池电解饱和食盐水的装置如下图所示,下列说法正确的是( )
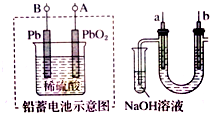

| A. | 铅蓄电池A极应与U形管中a极连接 | |
| B. | 铅蓄电池放电时溶液的pH值变小 | |
| C. | a电极用铁作电极,b电极用石墨作电极 | |
| D. | 实验结束后可将U型管、试管中的溶液倒入下水道 |
7.已知反应:A(g)+2B(g)?C(s)+D(?)△H<0,将A和B按下图比例充入一体积为10L的密闭容器中,经20s达到平衡,A、B物质浓度的变化曲线如下图所示.下列说法正确的是( )
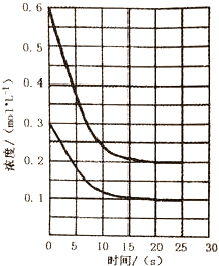

| A. | 从投料到20s时达到平衡,v(A)的反应速率为0.02mol•L-1•s-1 | |
| B. | 若该反应的化学平衡常数K=250,说明D的状态为气态 | |
| C. | 降低温度,有利于加快化学反应速率和提高反应的转化率 | |
| D. | 若D是固体且保持平衡的温度和压强不变,再向容器中充入3mol的B,则此时v正<v逆 |