题目内容
(没有过程不得分)实验室加热氯酸钾和二氧化锰的混合物制取氧气.若收集到标准状况下13.44L氧气,至少需要多少克氯酸钾?同时生成氯化钾的物质的量为多少?
考点:化学方程式的有关计算
专题:计算题
分析:发生2KClO3
2KCl+3O2↑,n(O2)=
=0.6mol,结合反应方程式计算.
| ||
| △ |
| 13.44L |
| 22.4L/mol |
解答:
解:标况下n(O2)=
=0.6mol,设生成KCl为xmol,消耗氯酸钾为ymol,则
2KClO3
2KCl+3O2↑,
2 2 3
y x 0.6mol
则x=
=0.4mol,
y=0.4mol,则氯酸钾的质量为0.4mol×122.5g/mol=49g,
答:至少需要49克氯酸钾,同时生成氯化钾的物质的量为0.4mol.
| 13.44L |
| 22.4L/mol |
2KClO3
| ||
| △ |
2 2 3
y x 0.6mol
则x=
| 2×0.6mol |
| 3 |
y=0.4mol,则氯酸钾的质量为0.4mol×122.5g/mol=49g,
答:至少需要49克氯酸钾,同时生成氯化钾的物质的量为0.4mol.
点评:本题考查化学反应方程式的计算,为高频考点,把握发生的反应及物质的量的关系为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
实验室需用240mL 0.1mol?L-1的硫酸铜溶液,现选取250mL容量瓶进行配制,以下操作能配制成功的是( )
| A、称取3.84 g CuSO4粉末,加入250 mL水 |
| B、称取6.25 g CuSO4?5H2O晶体,加水配成250 mL溶液 |
| C、称取4.0 g CuSO4粉末,加入250 mL水 |
| D、称取4.0 g CuSO4?5H2O晶体,加水配成250 mL溶液 |
某无色透明的强酸性溶液中,能大量共存的一组离子是( )
| A、K+、Na+、AlO2-、SO42- |
| B、Mg2+、Al3+、NO3-、SO42- |
| C、Na+、K+、SO42-、MnO4- |
| D、NH4+、Na+、HCO3-、NO3- |
图Ⅰ、Ⅱ分别是甲、乙两组同学将反应AsO43-+2I-+2H+═AsO33-+I2+H2O设计成的原电池装置,其中C1、C2均为碳棒.甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液.下列叙述中正确的是( )
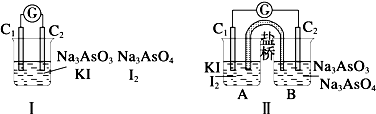

| A、甲组操作时,电流计(G)指针发生偏转 |
| B、乙组操作时,C1上发生的电极反应为 I2+2e-═2I- |
| C、甲组操作时,溶液颜色变浅 |
| D、乙组操作时,C2做正极 |
下列有关实验的说法不正确的是( )
| A、淀粉胶体中混有氯化钠杂质,可用半透膜做渗析实验提纯 |
| B、测定未知液的PH时,应该用干燥的PH试纸,否则一定会产生误差 |
| C、不用其它试剂即可鉴别稀盐酸和碳酸钠两种无色溶液 |
| D、熔融氢氧化钠不能在耐高温的石英坩埚中 |