题目内容
18.在无色透明强酸性溶液中,以下能大量共存的离子组是( )| A. | K+、Cu2+、NO3-、CO32- | B. | Mg2+、Na+、Cl-、SO42- | ||
| C. | Mg2+、NH4+、NO3-、CO32- | D. | NH4+、K+、OH-、SO42- |
分析 强酸溶液中含大量的氢离子,根据离子之间不能结合生成沉淀、气体、水等,不发生氧化还原反应等,则离子大量共存,并结合离子的颜色来解答.
解答 解:A.Cu2+为蓝色,与无色不符,且酸溶液中不能大量存在CO32-,故A不选;
B.酸溶液中该组离子之间不反应,可大量共存,且离子均为无色,故B选;
C.酸溶液中不能大量存在CO32-,故C不选;
D.酸溶液中不能大量存在OH-,且NH4+、OH-结合生成弱碱,不能共存,故D不选;
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
8.常温下,以下各组离子在有关限定条件下溶液中一定能大量共存的是( )
| A. | 由水电离产生的c(H+)=10-12 mol/L的溶液中:K+、Na+、Fe2+、NO3- | |
| B. | 在c(H+)=$\sqrt{{K}_{W}}$mol/L的溶液中:K+、Fe3+、HCO3-、AlO2- | |
| C. | 常温下,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:K+、AlO2-、SO42-、Cl- | |
| D. | pH=13的溶液中:NH4+、Na+、CO32-、SO42- |
9.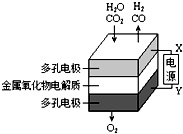 在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
 在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温共电解H2O~CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )| A. | X是电源的负极 | |
| B. | 阴极的反应式是:H2O+2eˉ═H2+O2- | |
| C. | 总反应可表示为:H2O+CO2═H2+CO+O2 | |
| D. | 阴、阳两极生成的气体的物质的量之比是2:1 |
6.向三份0.1mol•L-1 CH3COONa溶液中分别加入少量Na2SO3、NH4NO3、FeCl3固体(忽略溶液体积变化),则CH3COO-的浓度变化依次为( )
| A. | 减小、增大、减小 | B. | 增大、减小、减小 | C. | 减小、增大、增大 | D. | 增大、减小、增大 |
13.下列说法正确的是( )
| A. | 投入铁片产生H2的溶液中可大量存在H+、Mg2+、SO42-、NO3- | |
| B. | 将过量二氧化硫气体入冷氨水中:SO2+NH3•H2O═HSO3-+NH4+ | |
| C. | 1.0mol•L-1的KNO3溶液中可大量存在H+、Fe2+、Cl-、SO42- | |
| D. | 硫化铜溶于硝酸的离子方程式为CuS+2H+═H2S↑+Cu2+ |
10.下列物质的分类全部正确的是( )
| A. | NO2-酸性氧化物 Na2O2-碱性氧化物 Al2O3-两性氧化物 | |
| B. | 盐酸-混合物 胆矾-纯净物 C60-单质 | |
| C. | 纯碱-碱 硫化氢-酸 小苏打-酸式盐 | |
| D. | 液氯-非电解质 硫酸钡-强电解质 醋酸-弱电解质 |
7.有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子(每种物质只含一种阴离子且互不重复).
已知:①A、C溶液的pH均大于7,A、B的溶液中水的电离程度相同;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象.
(1)A是CH3COONa.
(2)25℃时,0.1mol•L-1 B溶液的pH=a,则B溶液中c(H+)-c(NH3•H2O)=1×10(a-14(用含有a的关系式表示).
(3)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序为c(OH-)> c(Ba2+)= c(Cl-)> c(NH4+)> c(H+).
(4)在一定体积的0.005mol•L-1的C溶液中,加入一定体积的0.001 25mol•L-1的盐酸时,混合溶液的pH=11,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是1:4.
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、Cl-、OH-、SO42- |
(1)A是CH3COONa.
(2)25℃时,0.1mol•L-1 B溶液的pH=a,则B溶液中c(H+)-c(NH3•H2O)=1×10(a-14(用含有a的关系式表示).
(3)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序为c(OH-)> c(Ba2+)= c(Cl-)> c(NH4+)> c(H+).
(4)在一定体积的0.005mol•L-1的C溶液中,加入一定体积的0.001 25mol•L-1的盐酸时,混合溶液的pH=11,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是1:4.
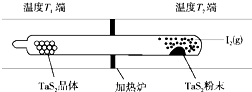 化学反应原理在科研和生产中有广泛应用.
化学反应原理在科研和生产中有广泛应用.