题目内容
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气.火箭残骸中常现红棕色气体,原因为
N2O4(g)?2NO2(g),当温度升高时,气体颜色变深,则该反应为 (填“吸热”或“放热”)反应;
(2)已知:①N2(g)+2O2(g)═N2O4(l)△H1=-19.5kJ?mol-1
②N2H4(1)+O2(g)═N2(g)+2H2O(g)△H2=-534.2kJ?mol-1
写出肼和N2O4反应的热化学方程式 ;
(3)肼-空气燃料电池中,电解质溶液为碱性,该电池放电时:
负极的反应式为 ;
正极的反应式为 .
(1)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气.火箭残骸中常现红棕色气体,原因为
N2O4(g)?2NO2(g),当温度升高时,气体颜色变深,则该反应为
(2)已知:①N2(g)+2O2(g)═N2O4(l)△H1=-19.5kJ?mol-1
②N2H4(1)+O2(g)═N2(g)+2H2O(g)△H2=-534.2kJ?mol-1
写出肼和N2O4反应的热化学方程式
(3)肼-空气燃料电池中,电解质溶液为碱性,该电池放电时:
负极的反应式为
正极的反应式为
考点:用盖斯定律进行有关反应热的计算,化学电源新型电池
专题:化学反应中的能量变化,电化学专题
分析:(1)升高温度,平衡向吸热反应方向移动;
(2)依据盖斯定律,结合题干热化学方程式计算写出;
(3)肼-氧气碱性燃料电池中,负极上燃料肼失电子和氢氧根离子反应生成水和氮气,正极氧气得电子形成氢氧根离子.
(2)依据盖斯定律,结合题干热化学方程式计算写出;
(3)肼-氧气碱性燃料电池中,负极上燃料肼失电子和氢氧根离子反应生成水和氮气,正极氧气得电子形成氢氧根离子.
解答:
解:(1)升高温度,化学平衡向吸热反应方向移动,当温度升高时,气体颜色变深,平衡向正反应方向移动,所以正反应是吸热反应;
故答案为:吸热;
(2)①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ?mol-1
②N2H4(l)+O2 (g)=N2(g)+2H2O(g)△H2=-534.2kJ?mol-1
根据盖斯定律写出肼和N2O4反应的热化学方程:②×2-①得到:2N2H4(l)++N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9kJ/mol;
故答案为:2N2H4(l)++N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9kJ/mol.
(3)肼-氧气碱性燃料电池中,负极上燃料肼失电子和氢氧根离子反应生成水和氮气,电极反应式为N2H4+4OH--4e-=4H2O+N2↑,正极发生还原反应,电极方程式为O2+2H2O+4e-=4OH-,故答案为:N2H4+4OH--4e-=4H2O+N2↑;O2+2H2O+4e-=4OH-.
故答案为:吸热;
(2)①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ?mol-1
②N2H4(l)+O2 (g)=N2(g)+2H2O(g)△H2=-534.2kJ?mol-1
根据盖斯定律写出肼和N2O4反应的热化学方程:②×2-①得到:2N2H4(l)++N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9kJ/mol;
故答案为:2N2H4(l)++N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9kJ/mol.
(3)肼-氧气碱性燃料电池中,负极上燃料肼失电子和氢氧根离子反应生成水和氮气,电极反应式为N2H4+4OH--4e-=4H2O+N2↑,正极发生还原反应,电极方程式为O2+2H2O+4e-=4OH-,故答案为:N2H4+4OH--4e-=4H2O+N2↑;O2+2H2O+4e-=4OH-.
点评:本题考查了平衡移动、热化学方程式的书写和燃料电池电极反应,综合性较强,中等难度.写电极反应注意介质的参与.

练习册系列答案
相关题目
下列各项表达中正确的是( )
A、-CH3(甲基)的电子式: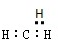 |
B、硝基苯的结构简式: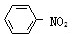 |
C、甲醛的结构式: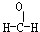 |
D、聚丙烯的结构简式: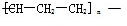 |
下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A、1 mol聚乙烯含有的原子数目为6NA |
| B、标况下1L己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA/22.4 |
| C、1 mol甲基含9NA个电子 |
| D、2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
将4.16g某Cu和Fe2O3的混合粉末投入到一定量的稀HNO3中,恰好完全反应,并生成标准状况下的NO体积为448mL,向反应完成后的溶液中滴加KSCN溶液,溶液不显红色,则原混合粉末中Fe2O3和Cu的物质的量之比为( )
| A、1:4 | B、1:1 |
| C、7:15 | D、4:1 |
烹鱼时加入少量的料酒和食醋可减少腥味.这是因为料酒中的乙醇与食醋中的乙酸发生了化学反应生成了有香味的乙酸乙酯的缘故.加一点酒和醋能使菜味香可口,原因是( )
| A、有盐类物质生成 |
| B、有酯类物质生成 |
| C、有醇类物质生成 |
| D、有酸类物质生成 |
有关NaHCO3 和Na2CO3 性质,以下叙述错误的是( )
| A、往饱和碳酸钠溶液中通入足量CO2 ,溶液变浑浊 |
| B、往同物质的量浓度的两种溶液中滴入等量酚酞,Na2CO3 溶液红色更深 |
| C、将澄清石灰水加入NaHCO3 溶液中不产生沉淀,加入Na2CO3 溶液中产生白色沉淀 |
| D、同物质的量浓度同体积的两种溶液与Ca(OH)2 反应均完全转变为CaCO3,Na2CO3溶液消耗的大于NaHCO3溶液 |