题目内容
13.草酸是一种重要的化工产品.某校化学兴趣小组拟在实验室用硝酸氧化淀粉水解液制备草酸并探究草酸的分解产物.Ⅰ.草酸的制备
该小组同学设计如图1所示装置(加热、搅拌和仪器固定装置均已略去)来制备草酸.
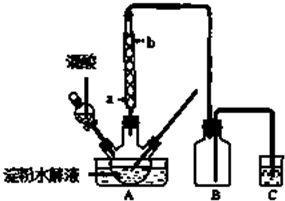
实验过程如下:
①将一定量的淀粉水解液加入三颈瓶中;
②控制反应液温度在55~60℃条件下,边搅拌边缓缓滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液;
③反应3h左右,冷却,抽滤后再重结晶得草酸晶体.
(1)该反应需控制反应液温度在55~60℃,并缓缓滴加混酸,原因是温度太低,则反应速率慢;温度太高或滴入过快会导致草酸产率下降(C6H12O6和H2C2O4进一步被氧化).
(2)抽滤是指利用抽气泵使抽滤瓶中的压强降低,达到固液分离的目的方法,抽滤的优点是可加快过滤速度,并能得到较干燥的沉淀.
(3)冷凝水的进口为a(a、b );
Ⅱ.草酸的分解实验探究
小组同学经查阅资料知,草酸晶体在101℃时熔化并开始升华,157℃时大量升华,继续升温会分解.为了检验草酸晶体受热分解的产物中是否有CO2,甲、乙两位同学分别设计了如图2的装置1、装置2来完成实验.
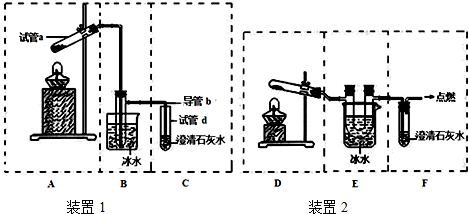
(4)简述检验装置1气密性的操作方法:如图连接好装置,将导管b没入水中,微热(或手捂)试管a,看到导管口处有气泡冒出,撤火(或松手)后,观察到导管内有一段水柱上升,则说明该装置的气密性良好.
(5)有同学提出装置B处可能会发生危险,理由是:B中的导管过长、过细,冷凝后的草酸晶体可能会堵塞导管而发生爆炸.
(6)甲、乙两位同学都考虑到了用冰水来冷凝,冰水冷凝的目的是:防止了草酸蒸气干扰CO2的检验.
(7)有同学提出甲、乙两位同学设计的装置都有缺陷,请你从A~F中选择合适的仪器,组装一套更合理的装置,按照气流由左到右的顺序依次为(用字母表示):AEF.
分析 Ⅰ.(1)温度低,反应速率慢,温度太高或滴加太快,会导致反应速率过快,且葡萄糖和操作能被氧化;
(2)抽滤可加快过滤速度,且能较大程度的除去水分;
(3)冷凝管中的水采用逆流方法;
Ⅱ.(4)利用空气热胀冷缩的性质来检查装置的气密性;
(5)草酸晶体受热升华,冷凝时会形成固体;
(6)草酸也能和氢氧化钙反应生成白色沉淀;
(7)加热固体时试管口要低于试管底;产生的气体中有草酸、一氧化碳,草酸也能和氢氧化钙反应生成白色沉淀,所以要除去草酸;一氧化碳有毒,不能直接排空;用澄清石灰水检验二氧化碳.
解答 解:Ⅰ.(1)温度低,反应速率慢,温度太高或滴加太快,会导致反应速率过快,且葡萄糖和操作能被氧化,从而降低草酸的产率,
故答案为:温度太低,则反应速率慢;温度太高或滴入过快会导致草酸产率下降(C6H12O6和H2C2O4进一步被氧化);
(2)抽滤可加快过滤速度,且能较大程度的除去水分,所以能得到较干燥的沉淀,
故答案为:可加快过滤速度,并能得到较干燥的沉淀;
(3)冷凝管中的水采用逆流方法,所以a为进水口、b为出水口,故答案为:a;
Ⅱ.(4)利用空气热胀冷缩的性质来检查装置的气密性,其检验方法为如图连接好装置,将导管b没入水中,微热(或手捂)试管a,看到导管口处有气泡冒出,撤火(或松手)后,观察到导管内有一段水柱上升,则说明该装置的气密性良好,
故答案为:如图连接好装置,将导管b没入水中,微热(或手捂)试管a,看到导管口处有气泡冒出,撤火(或松手)后,观察到导管内有一段水柱上升,则说明该装置的气密性良好;
(5)草酸易升华,得到的气体中含有草酸,如果B中的导管过长、过细,冷凝后的草酸晶体可能会堵塞导管而发生爆炸,
故答案为:B中的导管过长、过细,冷凝后的草酸晶体可能会堵塞导管而发生爆炸;
(6)草酸也能和氢氧化钙反应生成白色沉淀,草酸在冷却时生成固体,与二氧化碳分离,从而不干扰二氧化碳的检验,所以冷却的目的是防止了草酸蒸气干扰CO2的检验,
故答案为:防止了草酸蒸气干扰CO2的检验;
(7)加热固体时试管口要低于试管底,由于草酸在101℃时熔化,反应装置中试管口应向上倾斜,故选A装置;
产生的气体中有草酸、一氧化碳,选择装置E除去草酸,一氧化碳有毒,具有可燃性,可采用点燃的方法除去尾气中的一氧化碳,二氧化碳能使澄清石灰水变浑浊,因此一般用澄清石灰水检验二氧化碳的存在,故选装置F;所有组装一套可更好达到实验目的装置,按照气流由左到右的顺序依次为:A、E、F,
故答案为:AEF.
点评 本题考查物质制备,为高频考点,涉及仪器的使用、实验设计中仪器的选取、实验条件的确定等知识点,明确实验原理、物质的性质、仪器的用途等知识点是解本题关键,侧重考查学生实验设计、实验分析及知识的综合应用能力,高中学生对于抽滤装置了解较少,应该多加练习掌握,题目难度中等.

| A. | 2:7 | B. | 5:4 | C. | 1:1 | D. | 7:2 |
| A. | M/NA表示该气体单个分子的质量 | B. | mNA/M表示该气体的分子数 | ||
| C. | M/22.4表示该气体的密度 | D. | VM/mNA表示该气体一个分子的体积 |
| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
3mL浓硫酸,混匀后,投入几块碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品.
(1)浓硫酸的作用是催化剂、吸水剂;
(2)若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式C6H5CO18OH+CH3OH
 C6H5COOCH3+H218O.
C6H5COOCH3+H218O.(3)甲和乙两位同学分别设计了如图1所示的两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去).
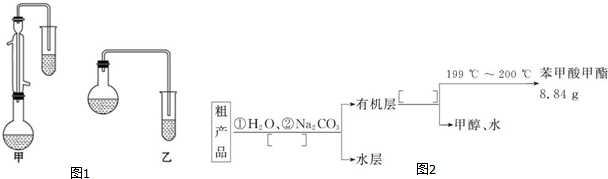
根据有机物的沸点,最好采用甲(填“甲”或“乙”)装置.理由是甲中有冷凝回流装置.
(4)反应物CH3OH应过量,理由是反应物CH3OH过量,使平衡向右移动,有利于提高苯甲酸的转化率.
Ⅱ.粗产品的精制
(5)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用如图2流程图进行精制,请在流程图中方括号内填入操作方法的名称.
(6)通过计算,苯甲酸甲酯的产率为65%.
| A. | KNO3 | B. | Ca(OH)2 | C. | BaSO4 | D. | AgCl |
 .
.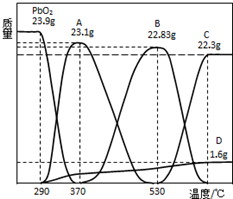 某种铅酸蓄电池具有廉价、长寿命、大容量的特点,它使用的电解质是可溶性的甲基磺酸铅,电池的工作原理:Pb(s)+PbO2(s)+2H2SO4(aq)$?_{充电}^{放电}$2PbSO4(s)+2H2O(l)
某种铅酸蓄电池具有廉价、长寿命、大容量的特点,它使用的电解质是可溶性的甲基磺酸铅,电池的工作原理:Pb(s)+PbO2(s)+2H2SO4(aq)$?_{充电}^{放电}$2PbSO4(s)+2H2O(l)