题目内容
8.某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅱ所示.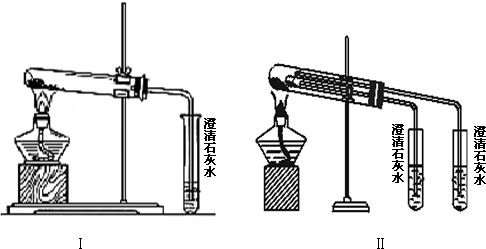
(1)图Ⅰ、Ⅱ所示实验均能鉴别这两种物质,与实验Ⅰ相比,实验Ⅱ的优点是(填选项序号)D.
A.Ⅱ比Ⅰ复杂 B.Ⅱ比Ⅰ安全
C.Ⅱ比Ⅰ难操作 D.Ⅱ可以做到用同一套装置进行对比实验,而Ⅰ不行
(2)若用实验Ⅱ验证碳酸钠和碳酸氢钠的稳定性.则试管B中应装入的固体最好是(填化学式)NaHCO3.
(3)某同学将质量为m1的NaHCO3固体放在试管中加热分解一段时间后,恢复到原条件,测得剩余固体的质量为m2.试管中发生的反应的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑生成的Na2CO3的质量为$\frac{53}{31}({m}_{1}-{m}_{2})$.
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应.当碳酸氢钠与氢氧化钙物质的量之比为2:1时,请设计实验检验反应后所得溶液中溶质的阴离子:取上层清液少许于洁净试管中,加入适量CaCl2溶液,若有白色沉淀生成,证明有CO32-.
分析 (1)根据两个实验的区别分析,Ⅱ可以做对比实验;
(2)不直接加热碳酸氢钠就能分解更说明碳酸氢钠不稳定;
(3)碳酸氢钠加热分解生成碳酸钠、二氧化碳气体和水,书写化学方程式,根据差量进行计算,由此分析解答;
(4)根据反应方程式判断溶液中的溶质;碳酸根离子能和钙离子反应生成碳酸钙白色沉淀,向上层清液中加入氯化钙溶液,若产生白色沉淀,就证明有碳酸根离子.
解答 解:(1)实验Ⅰ与实验Ⅱ相比,实验Ⅱ可以做到一套装置同时进行两个对比实验,而实验I不能,故选D,
故答案为:D;
(2)碳酸钠直接加热,碳酸氢钠不直接加热,不直接加热的碳酸氢钠能分解而直接加热的碳酸钠不分解更能说明碳酸氢钠不稳定,
故答案为:NaHCO3;
(3)碳酸氢钠加热发生的反应方程式为:2NaHO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,
根据差量法:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O△m
106 62
m(Na2CO3) (m1-m2)g
碳酸钠的质量为:m(Na2CO3)=$\frac{106({m}_{1}-{m}_{2})}{62}$g=$\frac{53}{31}({m}_{1}-{m}_{2})$,
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑; $\frac{53}{31}({m}_{1}-{m}_{2})$;
(4)碳酸氢钠与氢氧化钙的物质的量之比为2:1时,反应方程式为2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O,根据方程式知该溶液是碳酸钠溶液;该溶液中含有碳酸根离子,碳酸根离子能和钙离子生成白色沉淀,所以检验方法是:取上层清液于洁净的试管中加入适量CaCl2溶液,振荡,若有白色沉淀生成,则证明溶液中含有CO32-,
故答案为:取上层清液少许于洁净试管中,加入适量CaCl2溶液,若有白色沉淀生成,证明有CO32-.
点评 本题考查了NaHCO3性质实验方案的设计,题目难度中等,正确理解题干信息为解答关键,注意差量法的应用.

 通城学典默写能手系列答案
通城学典默写能手系列答案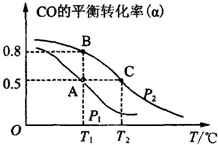 (1)已知:3H2(g)+3CO(g)═CH3OCH3(g)+CO2(g),△H=-247kJ/mol.一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是AE.
(1)已知:3H2(g)+3CO(g)═CH3OCH3(g)+CO2(g),△H=-247kJ/mol.一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是AE.a.低温高压 b.加入催化剂 c.体积不变充入氦气
d.增加CO的浓度 e.分离出二甲醚
(2)已知反应2CH3OH(g)═CH3OCH3(g)+H2O(g),在某温度下,在1L密闭容器中加入CH3OH,反应到10分钟时达到平衡,此时测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.01 | 0.2 | 0.2 |
②若加入CH3OH后,经10min反应达到平衡,该时间内反应速率v(CH3OH)=0.04 mol•L-1•min-1.若平衡后,再向容器中再加入0.01mol CH3OH和0.2mol CH3OCH3,此时正、逆反应速率的大小:v正> v逆 (填“>”、“<”或“=”).
(3)甲醇日趋成为重要的有机燃料,通常利用CO和H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g)═CH3OH(g).今在一容积可变的密闭容器中,充有10mol CO和20mol H2,用于合成甲醇.CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
①上述合成甲醇的反应为放热反应(填“放热”或“吸热”).
②A、B、C三点的平衡常数KA、KB、KC的大小关系为KA=KB>KC.
③若将达到平衡状态A时生成的甲醇用于构成甲醇一氧气燃料电池,电解质溶液为KOH浓溶液,则该电池工作时正极的电极反应式为O2+2H2O+4e-=4OH-.
| A. | 某物质焰色反应呈黄色,结论:该物质一定是钠盐 | |
| B. | 某溶液中滴加KSCN溶液,溶液不变红,再滴加氯水,变红,结论:原溶液一定有Fe2+ | |
| C. | 无色溶液中加入BaCl2溶液,有白色沉淀产生,再加稀硝酸,沉淀不消失,结论:原溶液一定含有SO42- | |
| D. | 无色溶液中加入稀盐酸,产生无色无味气体,该气体能使澄清石灰水变浑浊,结论:原溶液一定含有CO32- |
| A. | 氢氟酸 | B. | 浓盐酸 | C. | 溴水 | D. | 碘化银固体 |
| A. | 平衡时SO2的转化率:A>B | |
| B. | 可逆反应从开始到平衡放出的热量:A<B | |
| C. | 平衡时混合气体的总物质的量:A<B | |
| D. | 平衡时的化学反应速率:A>B |
NaBr+H2SO4→HBr+NaHSO4
CH3CH2OH+HBr?CH3CH2Br+H2O
CH3CH2CH2CH2OH+HBr?CH3CH2CH2CH2Br+H2O
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等.有关数据列表如下:
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g•cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
(1)溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是减少副产物烯和醚的生成,防止溴离子被浓硫酸氧化为溴单质.(填字母)
a.圆底烧瓶 b.量筒 c.温度计 d.普通漏斗
(2)制备实验中常采用80%的硫酸而不用98%的浓硫酸,其主要原因是减少副产物烯和醚的生成,防止溴离子被浓硫酸氧化为溴单质.
(3)在制备溴乙烷时,采用边反应边蒸出产物的方法,这样有利于平衡向生成溴乙烷的方向移动(或提高乙醇的转化率,提高溴乙烷的产率等);但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是1-溴丁烷的沸点和正丁醇相差较小,正丁醇会随1-溴丁烷同时蒸出.
(4)将制得的1-溴丁烷粗产品置于分液漏斗中,依次加入NaHSO3溶液和水,振荡、静置后,
1-溴丁烷在下层(填“上层”、“下层”或“不分层”),加入NaHSO3溶液的目的是除去产物中杂质溴.
(5)将实验(4)所得的1-溴丁烷粗产品干燥后,进行蒸馏操作,即可得到纯净的1-溴丁烷.
(6)某实验小组在制取1-溴丁烷的实验中所取1-丁醇(CH3CH2CH2CH2OH)7.4g.NaBr13.0g,最终制得1-溴丁烷9.6g,则1-溴丁烷的产率是70%.(保留2位有效数字)
| A. |  系统命名:2-乙基丙烷 系统命名:2-乙基丙烷 | |
| B. | 由分子式为C2H6O组成的物质一定是纯净物 | |
| C. | 正丁烷和异丁烷互为同系物 | |
| D. | 互为同系物的物质,在组成和结构上相似,所以化学性质也相似 |
 如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时颜色的变化.实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.填写下列空白.
如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时颜色的变化.实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.填写下列空白.