题目内容
4. 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如表:
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如表:| 化合物 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解度g/l00g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
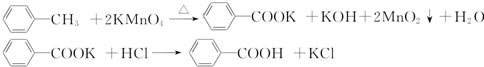
①在50mL三颈烧瓶中投入几粒沸石,将18.5mL正丁醇和13.4mL冰醋酸(过量),3~4滴浓硫酸按一定顺序均匀混合,安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管.
②将分水器分出的酯层和反应液一起倒入分液漏斗中依次用水洗,10% Na2CO3洗,再水洗,最后转移至锥形瓶并干燥.
③将干燥后的乙酸正丁酯加入烧瓶中,常压蒸馏,收集馏分,得15.1g乙酸正丁酯.
请回答有关问题:
(1)写出任意一种正丁醇同类的同分异构体的结构简式CH3CH2CH(OH)CH3.
(2)仪器A中发生反应的化学方程式为CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O.
(3)步骤①向三颈烧瓶中依次加入的药品是:正丁醇,浓硫酸,冰醋酸.
(4)步骤②中,用 10%Na2CO3溶液洗涤有机层,该步操作的目的是除去酯中混有的乙酸和正丁醇.
(5)步骤③在进行蒸馏操作时,若从118℃开始收集馏分,产率偏高,(填“高”或“低”)原因是会收集到少量未反应的冰醋酸和正丁醇.
(6)该实验生成的乙酸正丁酯的产率是65%.
分析 (1)丁醇同类的同分异构体,必须含有醇羟基,也可以看成是羟取代丁烷同分异构体上的氢;
(2)根据酯化反应原理酸脱羟基醇脱氢写出反应的化学方程式;
(3)先加密度小的药品,再加入密度较大的药品;
(4)乙酸丁酯不溶于饱和碳酸钠溶液,乙酸与碳酸钠反应而被吸收;
(5)若从118℃便开始收集馏分此时的蒸气中含有醋酸和正丁醇,会收集到少量未反应的冰醋酸和正丁醇,导致获得的乙酸正丁酯质量偏大;
(6)先根据酸的量计算理论上酯的量,再根据水的量计算酯的量,实际上酯的量与理论值之比即为酯的产率.
解答 解:(1)丁醇同类的同分异构体,必须含有醇羟基,也可以看成是羟取代丁烷同分异构体上的氢,其中一种的结构简式为:CH3CH2CH(OH)CH3,
故答案为:CH3CH2CH(OH)CH3;
(2)酯化反应的本质为酸脱羟基,醇脱氢,乙酸与丁醇在浓硫酸作用下加热发生酯化反应生成乙酸丁酯和水,该反应为可逆反应,化学方程式为:CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O,
故答案为:CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O;
(3)先加密度小的药品,再加入密度较大的药品,所以先后顺序为:正丁醇,浓硫酸,冰醋酸,
故答案为:正丁醇,浓硫酸,冰醋酸;
(4)乙酸丁酯不溶于饱和碳酸钠溶液,吸收正丁醇,乙酸与碳酸钠反应而被吸收,
故答案为:除去酯中混有的乙酸和正丁醇;
(5)若从118℃便开始收集馏分此时的蒸气中含有醋酸和正丁醇,会收集到少量未反应的冰醋酸和正丁醇,因此会导致产率偏高,
故答案为:高;会收集到少量未反应的冰醋酸和正丁醇;
(6)正丁醇的质量=0.8 g/mL×18.5mL=14.8g;冰醋酸的质量=1.045g/mL×13.4mL=14.003g;
理论上14.8g正丁醇完全反应生成酯的质量为xg,需乙酸的质量是yg.
乙酸和正丁醇的反应方程式为CH3COOH+CH3CH2CH2CH2OH(7)正丁醇的质量=0.8 g/mL×18.5mL=14.8g;冰醋酸的质量=1.045g/mL×13.4mL=14.003g;
理论上14.8g正丁醇完全反应生成酯的质量为xg,需乙酸的质量是yg.
乙酸和正丁醇的反应方程式为CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O
60g 74g 116g 18g
yg 14.8g xg
所以x=23.2 y=12g<14.003g 所以乙酸过量,
乙酸正丁酯的产率=$\frac{15.1g}{23.2g}$×100%≈65%.
故答案为:65%.
点评 本题主要考查了酯的制备,掌握酯的制备原理以及运用原理理解实验装置是解答的关键,题目难度中等.试题充分培养了学生的分析、理解能力及灵活应用所学知识的能力.

 天天向上口算本系列答案
天天向上口算本系列答案| A. | 在一定温度下AgCl水溶液中,Ag+和Cl-浓度的乘积是一个常数 | |
| B. | AgCl的Ksp=1.8×10-10 mol2•L-2,在任何含AgCl固体的溶液中,c(Ag+)=c(Cl-)且Ag+与Cl-浓度的乘积等于1.8×10-10 mol2•L-2 | |
| C. | 温度一定时,当溶液中Ag+和Cl-浓度的乘积等于Ksp值时,此溶液为AgCl的饱和溶液 | |
| D. | 向2.0mL浓度均为0.1mol•L-1的KCl、KI混合溶液中滴加1~2滴0.01mol•L-1 AgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp小 |
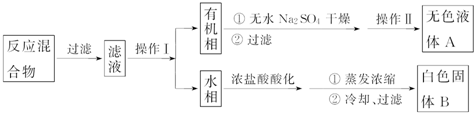
实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如图流程分离出苯甲酸和回收未反应的甲苯.
已知:苯甲酸分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物一般都有固定熔点.
(1)操作Ⅰ为分液,操作Ⅱ为蒸馏.
(2)无色液体A是甲苯,定性检验A的试剂是酸性KMnO4溶液,现象是溶液褪色.
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔.该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如表方案进行提纯和检验,实验结果表明推测正确.请在完成表中内容.
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中,加热溶解,冷却结晶,过滤 | 得到白色晶体和无色滤液 | |
| ② | 取少量滤液于试管中,滴入稀HNO3酸化的AgNO3溶液 | 生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体,取适量加热,测定熔点 | 白色晶体在122.4℃熔化为液体 | 白色晶体是苯甲酸 |
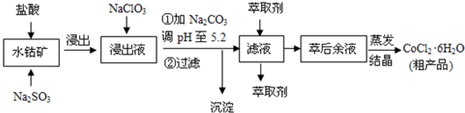
已知:
①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 |
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O
写出NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O.
不慎向“浸出液”中加了过量NaClO3,可能会生成有毒气体.写出生成该有毒气体的离子方程式ClO3-+5Cl-+6H+=3Cl2↑+3H2O.
(3)“加加Na2CO3调pH至a”,过滤所得到的沉淀成分为Fe(OH)3、Al(OH)3.加入萃取剂的目的是除去溶液中的Mn2+,防止Co2+转化为Co(OH)2沉淀.
(4)制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解.
(5)为测定粗产品中CoCl2•6H2O含量,称取一定质量的粗产品溶于水,加入足量HNO3酸化的AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水(答一条即可).
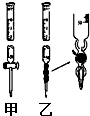 Ⅰ.(1)某学习小组用0.80mol/L标准浓度的氢氧化钠溶液测定未知浓度的盐酸.
Ⅰ.(1)某学习小组用0.80mol/L标准浓度的氢氧化钠溶液测定未知浓度的盐酸.①滴定管如图所示,用甲(填“甲”或“乙”)滴定管盛待测定的未知浓度的盐酸.
②用滴定的方法来测定盐酸的浓度,实验数据如下所示:
| 实验编号 | 待测盐酸溶液的体积/mL | 滴入NaOH溶液的体积/mL |
| 1 | 20.00 | 23.00 |
| 2 | 20.00 | 23.10 |
| 3 | 20.00 | 22.90 |
(2)若用酚酞作指示剂,达到滴定终点的标志是无色变浅红色且30s不变色
(3)以下操作可能造成测定结果偏高的是BC
A.盛装待测液的锥形瓶用水洗后未干燥
B.滴定前,碱式滴定管尖端有气泡,滴定后气泡消失
C.碱式滴定管用蒸馏水洗净后,未用标准氢氧化钠溶液润洗
D.读碱式滴定管的刻度时,滴定前仰视凹液面最低处,滴定后俯视读数
Ⅱ.为了测定某氯化锶(SrCl2)样品的纯度,探究活动小组同学设计了如下方案:
称取1.0g样品溶解于适量水中,向其中加入含AgNO3 2.38g的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应生成沉淀的离子),Cl-即被全部沉淀.然后用含Fe3+的溶液作指示剂,用0.2mol•L-1的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出,以测定氯化锶样品的纯度.
请回答下列问题:
(1)含Fe3+的溶液作指示剂达到滴定终点时发生颜色变化的离子方程式Fe3++3SCN-?Fe(SCN)3.
(2)在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+,需不断剧烈摇动锥形瓶,否则会使n(Cl-)的测定结果偏高(选填“偏高”“偏低”或“无影响”).
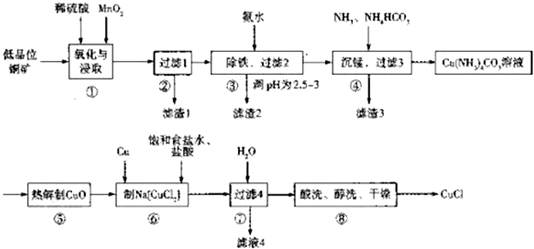
 .
.
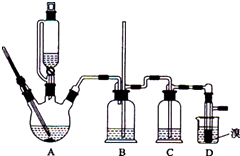 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下: