题目内容
某铁柱需长期浸入水下,为了减少腐蚀,下列措施中不能达到目的是( )
| A、在铁柱上铆上一些锌片 |
| B、制造铁柱时,向铁中渗入一定比例的铜制成合金 |
| C、在铁柱表面涂上一层较厚的沥青 |
| D、在铁柱表面镀锡 |
考点:金属防护的常用方法,金属的电化学腐蚀与防护
专题:电化学专题
分析:A、锌铁构成的原电池,金属锌是负极,铁是正极,正极金属被保护;
B、锌铜构成的原电池,金属铁是负极,铜是正极,正极金属被保护;
C、金属表面加保护层可以减慢金属的腐蚀;
D、锡的稳定性可以隔离铁与腐蚀介质接触.
B、锌铜构成的原电池,金属铁是负极,铜是正极,正极金属被保护;
C、金属表面加保护层可以减慢金属的腐蚀;
D、锡的稳定性可以隔离铁与腐蚀介质接触.
解答:
解:A、在铁柱上铆上一些锌片,这样锌铁构成的原电池,金属锌是负极,铁是正极,正极金属铁能被保护,能达到目的,故A错误;
B、制造铁柱时,向铁中渗入一定比例的铜制成合金,锌铜构成的原电池,金属铁是负极,铜是正极,铁易被腐蚀,不能达到目的,故B正确;
C、在铁柱表面涂上一层较厚的沥青,可以隔绝金属和空气、水的接触,能被保护,能达到目的,故C错误;
D、利用锡的稳定性隔离铁与腐蚀介质接触,可以减少铁的腐蚀,能达到目的,故D错误;
故选B.
B、制造铁柱时,向铁中渗入一定比例的铜制成合金,锌铜构成的原电池,金属铁是负极,铜是正极,铁易被腐蚀,不能达到目的,故B正确;
C、在铁柱表面涂上一层较厚的沥青,可以隔绝金属和空气、水的接触,能被保护,能达到目的,故C错误;
D、利用锡的稳定性隔离铁与腐蚀介质接触,可以减少铁的腐蚀,能达到目的,故D错误;
故选B.
点评:本题借助原电池的工作原理考查学生金属的腐蚀和防护知识,注意知识的迁移和应用是关键,难度不大.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH?CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是( )
| A、加少量烧碱溶液 | B、升高温度 |
| C、加少量冰醋酸 | D、加水 |
下列叙述不正确的是( )
| A、乙醇、乙烯和植物油都能使酸性高锰酸钾褪色 |
| B、乙醇、乙烷、乙酸都可以与钠反应生成氢气 |
C、聚丙烯的结构简式为: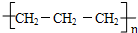 |
| D、用灼烧闻气味的方法可以区分纯棉织物和纯毛织物 |
已知碳酸、亚硫酸、次氯酸的平衡常数如表,下列说法正确的是( )
| H2CO3 | H2SO3 | HClO |
| K1=4.30×10-7 | K1=1.54×10-2 | K=2.95×10-8 |
| K2=5.61×10-11 | K2=1.02×10-7 |
| A、相同条件下,同浓度的NaClO溶液和Na2CO3溶液的碱性,前者更强 |
| B、Na2CO3溶液中通少量SO2:2CO32-+SO2+H2O═2HCO3-+SO32- |
| C、NaHCO3溶液中通少量SO2:2HCO3-+SO2═CO2+SO32-+H2O |
| D、向氯水中分别加入等浓度的NaHCO3和NaHSO3溶液,均可提高氯水中HClO的浓度 |
 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则
如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则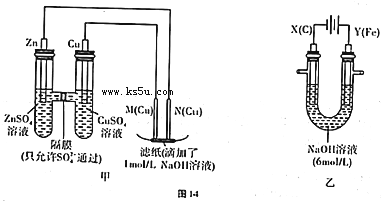
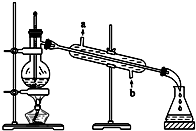 甘油的分离
甘油的分离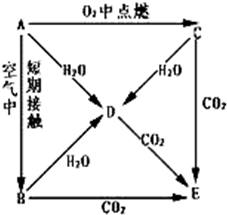 A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按图所示关系相互转化,已知A为单质.
A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按图所示关系相互转化,已知A为单质.