题目内容
向FeCl3的溶液中滴加KSCN溶液,溶液呈血红色,产生该现象的原因是生成了Fe(SCN)2+ …Fe(SCN)63-等其中的一种或多种配离子,可表示为Fe(SCN)x3-x(x=1~6).所谓配离子是由金属阳离子和一定数目的中性分子或阴离子以配位键结合而成的复杂离子.配离子和带相反电荷的离子组成的化合物叫配合物.
CuCl2与NaCl混合后也可生成配合物,该配合物能完全电离出Na+和配离子,配离子的电离则可忽略.为确定配离子的组成,每次取200mL5mol/L的CuCl2溶液,向其中加入NaCl固体,每次实验均充分反应,实验记录如下:
试计算在实验4所得溶液中配离子的浓度(假设加入NaCl固体后溶液体积不变)
CuCl2与NaCl混合后也可生成配合物,该配合物能完全电离出Na+和配离子,配离子的电离则可忽略.为确定配离子的组成,每次取200mL5mol/L的CuCl2溶液,向其中加入NaCl固体,每次实验均充分反应,实验记录如下:
| 实验序号 | 加入n(NaCl)/mol | 测得溶液中n(Cu2+)/mol | 测得溶液中n(Cl-)/mol |
| 1 | 3 | 0 | 1 |
| 2 | 2.4 | 0 | 0.4 |
| 3 | 2 | 0 | 0 |
| 4 | 1.2 | 0 | 0 |
| 5 | 1 | 0 | 0 |
| 6 | 0.4 | 0.2 | 0 |
考点:配合物的成键情况
专题:化学键与晶体结构
分析:200mL5mol/L的CuCl2中含有n(Cu2+)=0.2L×5mol/L=1mol,n(Cl-)=2mol,由实验1可知,加入3molNaCl后n(Cl-)=1mol,n(Cu2+)=0,因此配阴离子中n(Cu2+):n(Cl-)=1mol:(5-1)mol=1:4,配阴离子化学式为:CuCl42-,此配阴离子在实验2、3中均成立.根据实验5、6可知,配阴离子中n(Cu2+):n(Cl-)=1:3,所以,配离子为CuCl3-.
解答:
解:200mL5mol/L的CuCl2中含有n(Cu2+)=0.2L×5mol/L=1mol,n(Cl-)=2mol,由实验1可知,加入3molNaCl后n(Cl-)=1mol,n(Cu2+)=0,因此配阴离子中n(Cu2+):n(Cl-)=1mol:(5-1)mol=1:4,配阴离子化学式为:CuCl42-,此配阴离子在实验2、3中均成立.根据实验5、6可知,配阴离子中n(Cu2+):n(Cl-)=1:3,所以,配离子为CuCl3-.设n(CuCl3-)=xmol,则n(CuCl42-)=(1-x)mol,则3x+4(1-x)=2=1.2,解得x=0.8,即c(CuCl3-)=
=4 mol/L,c(CuCl42-)=
=1 mol/L.
故答案为:在实验4所得溶液中配离子c(CuCl3-)=4 mol/L,c(CuCl42-)=1 mol/L.
| 0.8mol |
| 0.2L |
| (1-0.8)mol |
| 0.2L |
故答案为:在实验4所得溶液中配离子c(CuCl3-)=4 mol/L,c(CuCl42-)=1 mol/L.
点评:本题重点考查计算能力以及看图提取信息、分析问题、解决问题的能力,难度很大.

练习册系列答案
相关题目
下列各组混合物,其总的物质的量均为a mol,组内各物质的物质的量以任意比混合,完全燃烧时消耗O2的量不变的是( )
| A、乙炔、乙醛、乙二醇 |
| B、乙烯、乙酸、葡萄糖 |
| C、乙烯、丁烯、环已烷 |
| D、乙烯、乙醇、丙烯酸 |
某铁柱需长期浸入水下,为了减少腐蚀,下列措施中不能达到目的是( )
| A、在铁柱上铆上一些锌片 |
| B、制造铁柱时,向铁中渗入一定比例的铜制成合金 |
| C、在铁柱表面涂上一层较厚的沥青 |
| D、在铁柱表面镀锡 |
反应 2A=B+3C,在20℃时进行,v(A)=5mol/(L?s),已知每升温10℃,该反应速率增大到原来的2倍,则当其它条件不变而温度升到50℃时,反应速率v(B)是( )
| A、20 mol/(L?s) |
| B、40 mol/(L?s) |
| C、60 mol/(L?s) |
| D、15 mol/(L?s) |
在1 100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g)△H=a kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是( )
| A、若生成1 mol Fe,则吸收的热量小于akJ |
| B、若要提高CO的转化率,则应该加入适当的过量Fe0 |
| C、若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| D、达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO2)=0.0263 mol/L |
09年是勒夏特列诞生189周年下列事实中,不能用勒夏特列原理解释的是( )
| A、在FeSO4溶液中加入少量铁粉以防止Fe2+被氧化 |
| B、合成氨工业上,采用高压以提高NH3的产率 |
| C、实验室中常用排饱和食盐水的方法收集Cl2 |
| D、工业生产硫酸的过程中使用过量的空气以提高SO2的利用率 |
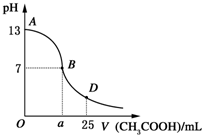 I.如图所示,向25mL 0.1mol?L-1 NaOH溶液中逐滴滴加0.2mol?L-1 CH3COOH溶液过程中溶液pH的变化曲线.请回答:
I.如图所示,向25mL 0.1mol?L-1 NaOH溶液中逐滴滴加0.2mol?L-1 CH3COOH溶液过程中溶液pH的变化曲线.请回答:
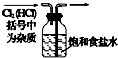
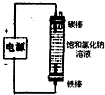
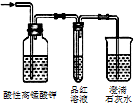
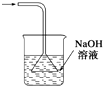
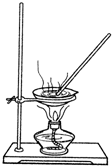 某研究性学习小组的同学设计一套方案,在实验室中制取肥皂(如图为硬脂酸甘油酯在碱性条件下水解的装置图)及甘油.已知酒精的沸点为78.5℃、甘油的沸点为290℃,硬脂酸甘油酯的沸点为260℃.
某研究性学习小组的同学设计一套方案,在实验室中制取肥皂(如图为硬脂酸甘油酯在碱性条件下水解的装置图)及甘油.已知酒精的沸点为78.5℃、甘油的沸点为290℃,硬脂酸甘油酯的沸点为260℃.