题目内容
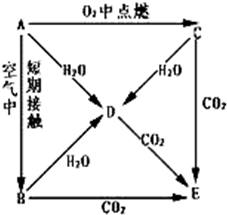 A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按图所示关系相互转化,已知A为单质.
A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按图所示关系相互转化,已知A为单质.(1)写出A→E的化学式:A
(2)写下列反应的离子方程式
A→D:
考点:无机物的推断
专题:推断题
分析:A为单质,由A
C可知,C为氧化物,由C
D,结合A
D可知,D只能为碱,A的元素为短周期元素,故A为Na,C为Na2O2,D为NaOH,由D
E,C
E可知,E为Na2CO3;
Na在空气中短期接触生成B,B为Na2O,Na2O与CO2反应生成Na2CO3,与水反应生成NaOH,符合转化关系.
| O2 |
| H2O |
| H2O |
| CO2 |
| CO2 |
Na在空气中短期接触生成B,B为Na2O,Na2O与CO2反应生成Na2CO3,与水反应生成NaOH,符合转化关系.
解答:
解:A为单质,由A
C可知,C为氧化物,由C
D,结合A
D可知,D只能为碱,A的元素为短周期元素,故A为Na,C为Na2O2,D为NaOH,由D
E,C
E可知,
E为Na2CO3;Na在空气中短期接触生成B,B为Na2O,Na2O与CO2反应生成Na2CO3,与水反应生成NaOH,符合转化关系,
(1)由上述分析可知,A为Na,B为Na2O,C为Na2O2,D为NaOH,E为Na2CO3,故答案为:Na;Na2O;Na2O2;NaOH;Na2CO3;
(2)A→D是钠与水反应生成氢氧化钠与氢气,反应的离子方程式为:2Na+2H2O=2Na++OH-+H2↑;
C→D是过氧化钠与水反应生成氢氧化钠与氧气,反应的离子方程式为:2Na2O2+2H2O=4Na++4OH-+O2↑,
D+CO2(过量)是氢氧化钠和过量二氧化碳反应生成碳酸氢钠,反应的离子方程式为:OH-+CO2=HCO3-;
故答案为:2Na+2H2O=2Na++2OH-+H2↑,2Na2O2+2H2O=4Na++4OH-+O2↑,OH-+CO2=HCO3-;
| O2 |
| H2O |
| H2O |
| CO2 |
| CO2 |
E为Na2CO3;Na在空气中短期接触生成B,B为Na2O,Na2O与CO2反应生成Na2CO3,与水反应生成NaOH,符合转化关系,
(1)由上述分析可知,A为Na,B为Na2O,C为Na2O2,D为NaOH,E为Na2CO3,故答案为:Na;Na2O;Na2O2;NaOH;Na2CO3;
(2)A→D是钠与水反应生成氢氧化钠与氢气,反应的离子方程式为:2Na+2H2O=2Na++OH-+H2↑;
C→D是过氧化钠与水反应生成氢氧化钠与氧气,反应的离子方程式为:2Na2O2+2H2O=4Na++4OH-+O2↑,
D+CO2(过量)是氢氧化钠和过量二氧化碳反应生成碳酸氢钠,反应的离子方程式为:OH-+CO2=HCO3-;
故答案为:2Na+2H2O=2Na++2OH-+H2↑,2Na2O2+2H2O=4Na++4OH-+O2↑,OH-+CO2=HCO3-;
点评:本题以无机框图题的形式考查Na元素单质及其化合物之间的相互转化关系、化学用语的书写等,比较基础,结合转化关系判断D为碱是关键,推断金属A为Na,然后进行验证.

练习册系列答案
相关题目
某铁柱需长期浸入水下,为了减少腐蚀,下列措施中不能达到目的是( )
| A、在铁柱上铆上一些锌片 |
| B、制造铁柱时,向铁中渗入一定比例的铜制成合金 |
| C、在铁柱表面涂上一层较厚的沥青 |
| D、在铁柱表面镀锡 |
在1 100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g)△H=a kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是( )
| A、若生成1 mol Fe,则吸收的热量小于akJ |
| B、若要提高CO的转化率,则应该加入适当的过量Fe0 |
| C、若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| D、达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO2)=0.0263 mol/L |
3He与4He互为同位素,下列说法不正确的是( )
| A、3He与4He具有相同的中子数 |
| B、3He与4He具有相同的质子数 |
| C、3He与4He具有相同的最外层电子数 |
| D、3He与4He具有不同的质量数 |
下列叙述中的前后两个量之比为1:2的是( )
| A、相同温度下,pH=12的Ba(OH)2与pH=12的KOH溶液中,c〔(Ba(OH)2〕:c(KOH) |
| B、相同温度下,0.1mol/L乙酸溶液与0.2mol/L乙酸溶液中,c(H+)之比 |
| C、常温下,氨水与(NH4)2SO4溶液混合后pH=7的溶液中,c(NH4+):c(SO42-) |
| D、液面在“0”刻度时,25mL碱式滴定管和50mL碱式滴定管所盛液体的体积 |
09年是勒夏特列诞生189周年下列事实中,不能用勒夏特列原理解释的是( )
| A、在FeSO4溶液中加入少量铁粉以防止Fe2+被氧化 |
| B、合成氨工业上,采用高压以提高NH3的产率 |
| C、实验室中常用排饱和食盐水的方法收集Cl2 |
| D、工业生产硫酸的过程中使用过量的空气以提高SO2的利用率 |
下列工业生产过程中,不涉及氧化还原反应的是( )
| A、用S制备H2SO4 |
| B、炼铁时用CaO除去原料中的SiO2 |
| C、将海水中的MgSO4转变为金属Mg |
| D、用NO2生产HNO3 |
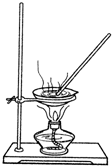 某研究性学习小组的同学设计一套方案,在实验室中制取肥皂(如图为硬脂酸甘油酯在碱性条件下水解的装置图)及甘油.已知酒精的沸点为78.5℃、甘油的沸点为290℃,硬脂酸甘油酯的沸点为260℃.
某研究性学习小组的同学设计一套方案,在实验室中制取肥皂(如图为硬脂酸甘油酯在碱性条件下水解的装置图)及甘油.已知酒精的沸点为78.5℃、甘油的沸点为290℃,硬脂酸甘油酯的沸点为260℃.