题目内容
夹紧以下装置中的弹簧夹并进行相关操作.下列情形中,表明相应装置漏气的是( )
A、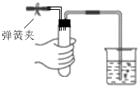 如图装置中,用手捂住试管,烧杯中出现气泡,手放开后,导管中形成一段稳定的水柱 |
B、 如图装置中,向长颈漏斗中加一定量水,并形成水柱,随后水柱下降至瓶中液面相平 |
C、 如图装置中,双手捂住烧瓶,导管中形成一段稳定的水柱,双手放开后,水柱慢慢回落 |
D、 如图装置中,将a管向上提至一段高度,a、b两管之间水面形成稳定的高度差 |
考点:化学实验方案的评价
专题:
分析:A.关闭弹簧夹,利用试管中空气的热胀冷缩检验气密性;
B.关闭弹簧夹,水柱下降至瓶中液面相平,说明装置漏气;
C.关闭弹簧夹,烧瓶中空气受热膨胀,导管中形成一段稳定的水柱,气密性良好;
D.关闭弹簧夹,a管向上提至一段高度,a、b两管之间水面形成稳定的高度差,气密性良好.
B.关闭弹簧夹,水柱下降至瓶中液面相平,说明装置漏气;
C.关闭弹簧夹,烧瓶中空气受热膨胀,导管中形成一段稳定的水柱,气密性良好;
D.关闭弹簧夹,a管向上提至一段高度,a、b两管之间水面形成稳定的高度差,气密性良好.
解答:
解:A.关闭弹簧夹,用手捂住试管,烧杯中出现气泡,手放开后,导管中形成一段稳定的水柱,则气密性良好,故A正确;
B.关闭弹簧夹,水柱下降至瓶中液面相平,说明装置漏气,若向长颈漏斗中加一定量水,并形成一段稳定的水柱,故B错误;
C.关闭弹簧夹,烧瓶中空气受热膨胀,导管中形成一段稳定的水柱,气密性良好,装置及操作合理,故C正确;
D.关闭弹簧夹,a管向上提至一段高度,a、b两管之间水面形成稳定的高度差,气密性良好,装置及操作合理,故D正确;
故选B.
B.关闭弹簧夹,水柱下降至瓶中液面相平,说明装置漏气,若向长颈漏斗中加一定量水,并形成一段稳定的水柱,故B错误;
C.关闭弹簧夹,烧瓶中空气受热膨胀,导管中形成一段稳定的水柱,气密性良好,装置及操作合理,故C正确;
D.关闭弹簧夹,a管向上提至一段高度,a、b两管之间水面形成稳定的高度差,气密性良好,装置及操作合理,故D正确;
故选B.
点评:本题考查化学实验方案的评价,为高频考点,侧重气密性检验的实验方法考查,把握加热法、液柱法的操作及现象为解答的关键,注重实验操作的考查,题目难度不大.

练习册系列答案
相关题目
某有机物是药物生产的中间体,其结构简式如右图.下列有关叙述不正确的是( )


| A、该有机物与浓溴水可发生取代反应 |
| B、1 mol该有机物与足量NaOH溶液反应最多消耗4 mol NaOH |
| C、该有机物与浓硫酸混合共热可发生消去反应 |
| D、该有机物经催化氧化后与新制氢氧化铜悬浊液共热生成砖红色沉淀 |






 )可由下列路线合成:
)可由下列路线合成:
