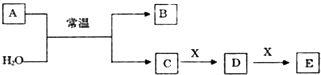
题目内容
请根据化学学科中的基本理论,回答下列问题
(1)纳米级的Cu2O可作为太阳光分解水的催化剂.火法还原CuO可制得Cu2O.已知:1克C(s)燃烧全部生成CO时放出热量9.2kJ;Cu2O(s)与O2(g)反应的能量变化如图1所示;请写出用足量炭粉还原CuO(s)制备Cu2O(s)的热化学方程式
(1)2CuO(s)+C(s)=CO(g)+Cu2O(s),△H=+35.6kJ?mol-1
(2)4Cu(OH)2+N2H4=2Cu2O+N2+6H2O

(2)在加热条件下用液态肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时生成N2和H2O.该反应的化学方程式为 ,当生成N211.2L(已换算为标准状况)时,可制备纳米级Cu2O的质量为
(3)某兴趣小组同学以纳米级Cu2O催化光解水蒸气并探究外界条件对化学平衡的影响.
①在体积均为1L,温度分别为T1、T2的A、B两密闭容器中都加入纳米级Cu2O并通人0.1mol水蒸气,发生反应:2H2O(g)?2H2(g)+O2(g)△H=+484kJ?mol-1经测定A、B两容器在反应过程中发生如图2所示变化,则A、B两容器反应的温度T1 T2 (填“<”、“=”或“>”),该过程中A容器至少需要吸收能量 kJ
②当该反应处于平衡状态时,下列既能增大反应速率,又能增大H2O(g)分解率的措施是(填序号)
A.向平衡混合物中充入Ar B.升高反应的温度
C.增大反应体系的压强 D.向平衡混合物中充人O2
(4)25℃时,H2SO3═HSO3-+H+的电离常数Ka=1×10-2mol/L,则该温度下NaHSO3的水解平衡常数Kh= mol/L.
(1)纳米级的Cu2O可作为太阳光分解水的催化剂.火法还原CuO可制得Cu2O.已知:1克C(s)燃烧全部生成CO时放出热量9.2kJ;Cu2O(s)与O2(g)反应的能量变化如图1所示;请写出用足量炭粉还原CuO(s)制备Cu2O(s)的热化学方程式
(1)2CuO(s)+C(s)=CO(g)+Cu2O(s),△H=+35.6kJ?mol-1
(2)4Cu(OH)2+N2H4=2Cu2O+N2+6H2O

(2)在加热条件下用液态肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时生成N2和H2O.该反应的化学方程式为
(3)某兴趣小组同学以纳米级Cu2O催化光解水蒸气并探究外界条件对化学平衡的影响.
①在体积均为1L,温度分别为T1、T2的A、B两密闭容器中都加入纳米级Cu2O并通人0.1mol水蒸气,发生反应:2H2O(g)?2H2(g)+O2(g)△H=+484kJ?mol-1经测定A、B两容器在反应过程中发生如图2所示变化,则A、B两容器反应的温度T1
②当该反应处于平衡状态时,下列既能增大反应速率,又能增大H2O(g)分解率的措施是(填序号)
A.向平衡混合物中充入Ar B.升高反应的温度
C.增大反应体系的压强 D.向平衡混合物中充人O2
(4)25℃时,H2SO3═HSO3-+H+的电离常数Ka=1×10-2mol/L,则该温度下NaHSO3的水解平衡常数Kh=
考点:热化学方程式,化学平衡的影响因素,弱电解质在水溶液中的电离平衡
专题:基本概念与基本理论
分析:(1)分析图象结合热化学方程式和盖斯定律解答.
(2)液态肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时生成N2和H2O,根据原子守恒书写化学方程式,根据电子转移数目守恒计算;
(3)①依据化学方程式结合图象中t1中氢气含量计算分析;
②既能增大反应速率,又能增大H2O(g)分解率的条件为升温,减压,依据平衡移动原理分析判断;
(4)Ka=
,HSO3-+H2O?H2SO3+OH-,Kb=
,据此计算.
(2)液态肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时生成N2和H2O,根据原子守恒书写化学方程式,根据电子转移数目守恒计算;
(3)①依据化学方程式结合图象中t1中氢气含量计算分析;
②既能增大反应速率,又能增大H2O(g)分解率的条件为升温,减压,依据平衡移动原理分析判断;
(4)Ka=
| c(HSO3-)?c(H+) |
| c(H2SO3) |
| c(H2SO3)?Kw |
| c(HSO3-)?c(H+) |
解答:
解:(1)已知:1g C(s)燃烧全部生成CO时放出热量9.2kJ;24gC燃烧生成一氧化碳放热220.8KJ,热化学方程式为:2C(s)+O2(g)=2CO(g)△H=-220.8kJ?mol-1,依据图象书写热化学方程式2Cu2O(s)+O2(g)=4CuO(s)△H=-292kJ?mol-1;
①2Cu2O(s)+O2(g)=4CuO(s)△H=-292kJ?mol-1
②2C(s)+O2(g)=2CO(g)△H=-220.8kJ?mol-1
根据盖斯定律,②-①得4CuO(s)+2C(s)=2CO(g)+2Cu2O(s)△H=+71kJ?mol-1,
即2CuO(s)+C(s)=CO(g)+Cu2O(s)△H=+35.6kJ?mol-1,
故答案为:2CuO(s)+C(s)=CO(g)+Cu2O(s)△H=+35.6kJ?mol-1;
(2)用液态肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时生成N2和H2O,反应的化学方程式为:4Cu(OH)2+N2H4=2Cu2O+N2+6H2O,令生成的Cu2O的物质的量为nmol,根据电子转移数目守恒,则有nmol×2×(1-0)=
×2×[0-(-2)],解得n=1mol;
所以可制备Cu2O的质量为1mol×144g/mol=144g,
故答案为:4Cu(OH)2+N2H4=2Cu2O+N2+6H2O;144g;
(3)①依据化学方程式计算;依据图象中氢气百分含量为50%,设反应的水的物质的量为x
2H2O(g)
2H2(g)+O2 △H=484kJ?mol-1
2mol 484KJ
x x 0.5x
=50%,
计算得到x=
mol;反应放热=
kJ=16.1kJ;
水的分解率=
×100%=66,7%,和T2温度下水的分解率为50%,反应是吸热反应,温度越高水的分解率越大;所以T1>T2;
故答案为:>;16.1;
②既能增大反应速率,又能增大H2O(g)分解率的条件为升温,减压,
A.向平衡混合物中充入Ar,增大体系压强,平衡逆向进行,故A不符合;
B.反应是吸热反应,升高反应的温度,反应速率增大,平衡正向进行,水的分解率增大,故B符合;
C.反应是气体体积增大的反应,增大反应体系的压强,平衡逆向进行,故C不符合;
D.向平衡混合物中充人O2,平衡逆向进行,故D不符合;
故答案为:B;
(4)25℃时,H2SO3?HSO3-+H+的电离常数Ka=1×10-2mol/L,Ka=
,HSO3-+H2O?H2SO3+OH-,Kb=
=1.0×102×1.0×10-14=1.0×10-12;则该温度下NaHSO3的水解平衡常数Kh=1.0×10-12,故答案为:1.0×10-12.
①2Cu2O(s)+O2(g)=4CuO(s)△H=-292kJ?mol-1
②2C(s)+O2(g)=2CO(g)△H=-220.8kJ?mol-1
根据盖斯定律,②-①得4CuO(s)+2C(s)=2CO(g)+2Cu2O(s)△H=+71kJ?mol-1,
即2CuO(s)+C(s)=CO(g)+Cu2O(s)△H=+35.6kJ?mol-1,
故答案为:2CuO(s)+C(s)=CO(g)+Cu2O(s)△H=+35.6kJ?mol-1;
(2)用液态肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时生成N2和H2O,反应的化学方程式为:4Cu(OH)2+N2H4=2Cu2O+N2+6H2O,令生成的Cu2O的物质的量为nmol,根据电子转移数目守恒,则有nmol×2×(1-0)=
| 11.2L |
| 22.4L/mol |
所以可制备Cu2O的质量为1mol×144g/mol=144g,
故答案为:4Cu(OH)2+N2H4=2Cu2O+N2+6H2O;144g;
(3)①依据化学方程式计算;依据图象中氢气百分含量为50%,设反应的水的物质的量为x
2H2O(g)
| ||
| 氧化亚铜 |
2mol 484KJ
x x 0.5x
| x |
| 0.1mol-x+x+0.5x |
计算得到x=
| 1 |
| 15 |
| ||
| 2 |
水的分解率=
| ||
| 0.1 |
故答案为:>;16.1;
②既能增大反应速率,又能增大H2O(g)分解率的条件为升温,减压,
A.向平衡混合物中充入Ar,增大体系压强,平衡逆向进行,故A不符合;
B.反应是吸热反应,升高反应的温度,反应速率增大,平衡正向进行,水的分解率增大,故B符合;
C.反应是气体体积增大的反应,增大反应体系的压强,平衡逆向进行,故C不符合;
D.向平衡混合物中充人O2,平衡逆向进行,故D不符合;
故答案为:B;
(4)25℃时,H2SO3?HSO3-+H+的电离常数Ka=1×10-2mol/L,Ka=
| c(HSO3-)?c(H+) |
| c(H2SO3) |
| c(H2SO3)?Kw |
| c(HSO3-)?c(H+) |
点评:本题考查了热化学方程式的书写方法和盖斯定律的计算应用,化学平衡影响因素分析判断,水解常数与电离平衡常数的计算,注意平衡建立的条件分析应用,题目难度中等.

练习册系列答案
相关题目
 在100mL 0.1mol?L-1铝氨矾[NH4Al(SO4)2?12H2O]的水溶液中,逐滴滴入0.1mol?L-1的Ba(OH)2溶液,所得沉淀的质量与Ba(OH)2溶液的体积曲线如图所示[已知Ba(AlO2)2易溶易电离].下列说法正确的是( )
在100mL 0.1mol?L-1铝氨矾[NH4Al(SO4)2?12H2O]的水溶液中,逐滴滴入0.1mol?L-1的Ba(OH)2溶液,所得沉淀的质量与Ba(OH)2溶液的体积曲线如图所示[已知Ba(AlO2)2易溶易电离].下列说法正确的是( )| A、a点溶液中大量存在的离子有NH4+和SO42- |
| B、b点溶液中c(NH3?H2O)约为0.1mol?L-1 |
| C、a→b过程中,反应的只有SO42- |
| D、b→c过程中,反应的是Al(OH)3和NH4+ |
下列说法错误的是( )
| A、核磁共振氢谱图上可以推知有机物分子中有几种不同类型的氢原子及它们的数目 |
| B、红外光谱是用高能电子流等轰击样品分子,使分子失去电子变成分子离子或碎片离子 |
| C、质谱法具有快速、微量、精确的特点 |
| D、通过红外光谱可以测知有机物所含的官能团 |
苹果酸的结构简式如图所示,下列说法错误的是( )


| A、苹果酸中能发生酯化反应的官能团的数目有3个 |
| B、1mol苹果酸可与2molNaOH发生中和反应 |
| C、1mol苹果酸与足量金属Na反应生成1.5molH2 |
| D、H OOCCH2-CH(COOH)-OH与苹果酸是不同种物质 |
在给定的四种溶液中,含有以下各种微粒,一定能大量共存的是( )
| A、饱和Na2CO3 溶液中:Ca2+、NH4+、HCO3-、Cl- |
| B、常温下葡萄糖溶液中:SCN-、Cl-、K+、NH4+ |
| C、溴水中:Na+、CO32-、NH4+、SO42- |
| D、pH大于7的溶液:Na+、Ba2+、SO32-、ClO- |
夹紧以下装置中的弹簧夹并进行相关操作.下列情形中,表明相应装置漏气的是( )
A、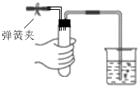 如图装置中,用手捂住试管,烧杯中出现气泡,手放开后,导管中形成一段稳定的水柱 |
B、 如图装置中,向长颈漏斗中加一定量水,并形成水柱,随后水柱下降至瓶中液面相平 |
C、 如图装置中,双手捂住烧瓶,导管中形成一段稳定的水柱,双手放开后,水柱慢慢回落 |
D、 如图装置中,将a管向上提至一段高度,a、b两管之间水面形成稳定的高度差 |