题目内容
6.通过以下反应可获得新型能源二甲醚(CH3OCH3 ).下列说法不正确的是①C(s)+H2O(g)═CO(g)+H2 (g)△H1=a kJ•mol-1
②CO(g)+H2O(g)═CO2(g)+H2 (g)△H2=b kJ•mol-1
③CO2 (g)+3H2 (g)═CH3OH(g)+H2O(g)△H3=c kJ•mol-1
④2CH3OH(g)═CH3OCH3 (g)+H2O(g)△H4=d kJ•mol-1( )
| A. | 反应①、②为反应③提供原料气 | |
| B. | 反应③也是 CO2资源化利用的方法之一 | |
| C. | 反应CH3OH(g)═$\frac{1}{2}$CH3OCH3 (g)+$\frac{1}{2}$H2O(l)的△H=$\frac{d}{2}$kJ•mol-1 | |
| D. | 反应 2CO(g)+4H2 (g)═CH3OCH3 (g)+H2O(g)的△H=( 2b+2c+d ) kJ•mol-1 |
分析 A.反应③中的反应物为CO2、H2;
B.反应③中的反应物为CO2,转化为甲醇;
C.由反应④可知,物质的量与热量成正比,且气态水的能量比液态水的能量高;
D.由盖斯定律可知,②×2+③×2+④得到2CO(g)+4H2 (g)═CH3OCH3 (g)+H2O(g).
解答 解:A.反应③中的反应物为CO2、H2,由反应可知,反应①、②为反应③提供原料气,故A正确;
B.反应③中的反应物为CO2,转化为甲醇,则反应③也是 CO2资源化利用的方法之一,故B正确;
C.由反应④可知,物质的量与热量成正比,且气态水的能量比液态水的能量高,则反应CH3OH(g)═$\frac{1}{2}$CH3OCH3 (g)+$\frac{1}{2}$H2O(l)的△H≠$\frac{d}{2}$kJ•mol-1,故C错误;
D.由盖斯定律可知,②×2+③×2+④得到2CO(g)+4H2 (g)═CH3OCH3 (g)+H2O(g),则△H=( 2b+2c+d ) kJ•mol-1,故D正确;
故选C.
点评 本题考查反应热与焓变,为高频考点,把握反应的特点、反应中能量变化、盖斯定律应用为解答的关键,侧重分析能力和应用能力的考查,题目难度中等.

练习册系列答案
相关题目
11.化学与生活密切相关.下列说法错误的是( )
| A. | PM2.5是指粒径不大于2.5μm的可吸入悬浮颗粒物 | |
| B. | 绿色化学要求从源头上消除或减少生产活动对环境的污染 | |
| C. | 燃煤中加入CaO可以减少酸雨的形成及温室气体的排放 | |
| D. | 天然气和液化石油气是我国目前推广使用的清洁燃料 |
6.H2O2分解速率受多种因素影响.实验测得 70℃时不同条件下H2O2浓度随时间的变化如图所示.下列说法正确的是( )
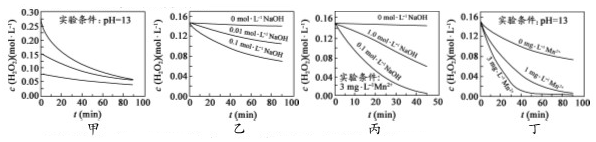

| A. | 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快 | |
| B. | 图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快 | |
| C. | 图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快 | |
| D. | 图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大 |
14.化学是建立在实验基础上的学科.关于下列各实验装置的叙述中,不正确的是( )

| A. | 装置①可用于实验室制取少量 NH3或 O2 | |
| B. | 可用从 a 处加水的方法检验装置②的气密性 | |
| C. | 实验室可用装置③收集 H2、NH3 | |
| D. | 利用装置④制硫酸和氢氧化钠,其中 b 为阳离子交换膜、c 为阴离子交换膜 |
1.下列说法正确的是( )
| A. | 石油液化气的主要成份为甲烷 | |
| B. | 燃料的脱硫、脱氮都是减少酸雨产生的措施 | |
| C. | BaSO4难溶于水是弱电解质,在医学上用作钡餐 | |
| D. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
3.合理利用燃料减小污染符合“绿色化学”理念,下列关于燃料的说法正确的是( )
| A. | “可燃冰”是将水变为油的新型燃料 | |
| B. | 氢气是具有热值高、无污染等优点的燃料 | |
| C. | 天然气、海洋能、太阳能、生物质能、风能、氢能 都属于新能源 | |
| D. | 电能是一次能源 |
20.乙醇中的化学键如图,则下列说法中正确的是( )
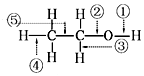

| A. | 当乙醇发生催化氧化时,被破坏的键是②③ | |
| B. | 当乙醇与Na反应时,被破坏的键是① | |
| C. | 当乙醇与乙酸反应时,被破坏的键是② | |
| D. | 当乙醇发生催化氧化时,被破坏的键是①④ |
1. X、Y、Z是一种短周期元素,原子半径的大小为:r(Y)>r(X)>r(Z),三种元素的原子序数之和为16;X、Y、Z三种元素的常见单质在适当条件下可发生如图转化关系.其中R为10电子分子,是一种常见的无机溶剂.下列说法中不正确的是( )
X、Y、Z是一种短周期元素,原子半径的大小为:r(Y)>r(X)>r(Z),三种元素的原子序数之和为16;X、Y、Z三种元素的常见单质在适当条件下可发生如图转化关系.其中R为10电子分子,是一种常见的无机溶剂.下列说法中不正确的是( )
 X、Y、Z是一种短周期元素,原子半径的大小为:r(Y)>r(X)>r(Z),三种元素的原子序数之和为16;X、Y、Z三种元素的常见单质在适当条件下可发生如图转化关系.其中R为10电子分子,是一种常见的无机溶剂.下列说法中不正确的是( )
X、Y、Z是一种短周期元素,原子半径的大小为:r(Y)>r(X)>r(Z),三种元素的原子序数之和为16;X、Y、Z三种元素的常见单质在适当条件下可发生如图转化关系.其中R为10电子分子,是一种常见的无机溶剂.下列说法中不正确的是( )| A. | X元素位于周期表中第16列 | |
| B. | X、Y、Z元素两两之间均能形成原子个数比为l:2的化合物 | |
| C. | X、Y、Z元素形成的化合物溶于水中,对水的电离平衡一定起抑制作用 | |
| D. | R和M的化学键类型和晶体类型都相同. |

 .
.  .
. $→_{K_{2}CO_{3}}^{(CH_{3})_{2}SO_{4}}$
$→_{K_{2}CO_{3}}^{(CH_{3})_{2}SO_{4}}$ (R代表烃基,R'代表烃基或H) 请写出以
(R代表烃基,R'代表烃基或H) 请写出以 和(CH3)2SO4为原料制备
和(CH3)2SO4为原料制备 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).