题目内容
8.在1.5mol Na2SO4中,含有的Na+数是( )| A. | 1.806×1024 | B. | 9.03×1023 | C. | 1.5 | D. | 3 |
分析 根据Na2SO4的化学式可知,钠离子物质的量为硫酸钠物质的量的2倍,由N=nNA计算.
解答 解:在1.5mol Na2SO4中Na+的物质的量是1.5mol×2=3mol,则含有的Na+数是3mol×6.02×1023mol-1=1.806×1024,
故选A.
点评 本题考查物质的量有关计算,比较基础,注意根据化学式判断含有微粒与物质的物质的量关系.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案
相关题目
18.向100mL0.1mol/L的硫酸铝溶液中滴加0.5mol/L的氢氧化钠溶液,如果得到1.17g沉淀,则消耗的氢氧化钠溶液的体积为( )
| A. | 130ml | B. | 100ml | C. | 90ml | D. | 50ml |
16.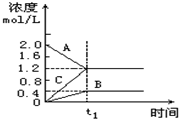 在一定的温度和容积为l L的密闭容器中投入A、B、C三种气态物质的浓度随时间的变化情况如图所示,下列结论中不正确的是( )
在一定的温度和容积为l L的密闭容器中投入A、B、C三种气态物质的浓度随时间的变化情况如图所示,下列结论中不正确的是( )
 在一定的温度和容积为l L的密闭容器中投入A、B、C三种气态物质的浓度随时间的变化情况如图所示,下列结论中不正确的是( )
在一定的温度和容积为l L的密闭容器中投入A、B、C三种气态物质的浓度随时间的变化情况如图所示,下列结论中不正确的是( )| A. | t1时刻之后,若再加入一定量的A,达平衡时A的转化率降低 | |
| B. | t1时刻之后,3v(A)逆=2v(C)正 (v-速率) | |
| C. | t1时刻之后,若升高温度,混合气体的平均摩尔质量增大,则该反应A消耗的方向为吸热反应 | |
| D. | 在温度和容积固定不变的条件下,起始投入1molB、3molC达平衡时A的体积分数为3/7 |
3.将19gKOH和KHCO3的混合物,在260℃时煅烧充分反应,冷却后称量,固体质量减少0.98g,则混合物中KOH和KHCO3的物质的量关系正确的是( )
| A. | n(KOH)=n(KHCO3) | B. | n(KOH)<n(KHCO3) | C. | n(KOH)>n(KHCO3) | D. | KOH、KHCO3任意比 |
13.将30mL5mol/L NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为( )
| A. | 0.3 mol/L | B. | 3 mol/L | C. | 0.15 mol/L | D. | 1.5 mol/L |
18.等质量的N2和CO中,有可能不相等的是( )
| A. | 物质的量 | B. | 体积 | C. | 分子数 | D. | 原子数 |