题目内容
核电荷数小于18的某元素X,其原子的电子层数n,最外层电子数为(2n+1),原子核内质子数为(2n2-1).下列关于元素X的说法中,不正确的是( )
| A、其最高化合价为+3价 |
| B、可以形成化学式为KXO3的盐 |
| C、其氢化物可以用来做喷泉实验 |
| D、其最高价氧化物的水化物是强酸 |
考点:原子结构与元素周期律的关系
专题:
分析:根据核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数是2n2-1.
假设n=1时,最外层电子数为3,不符合题意;
n=2时,最外层电子数为5,质子数为7,符合题意;
n=3时,最外层电子数为7,质子数为17,符合题意,以此来解答.
假设n=1时,最外层电子数为3,不符合题意;
n=2时,最外层电子数为5,质子数为7,符合题意;
n=3时,最外层电子数为7,质子数为17,符合题意,以此来解答.
解答:
解:根据核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数是2n2-1.假设n=1时,最外层电子数为3,不符合题意;n=2时,最外层电子数为5,质子数为7,X为N元素,符合题意;n=3时,最外层电子数为7,质子数为17,X为Cl元素,符合题意,
A.X可能为N或Cl,最高化合物为+5价或+7价,故A错误;
B.元素X可能为氮元素或氯元素,可形成KNO3或KClO3,故B正确;
C.对应的氢化物为氨气或氯化氢,都易溶于水,可形成喷泉,故C正确;
D.对应的最高价氧化物的水化物为硝酸或高氯酸,都为强酸,故D正确.
故选A.
A.X可能为N或Cl,最高化合物为+5价或+7价,故A错误;
B.元素X可能为氮元素或氯元素,可形成KNO3或KClO3,故B正确;
C.对应的氢化物为氨气或氯化氢,都易溶于水,可形成喷泉,故C正确;
D.对应的最高价氧化物的水化物为硝酸或高氯酸,都为强酸,故D正确.
故选A.
点评:本题考查原子结构中电子层数、最外层电子数、质子数的关系,利用假设法令n分别为1、2、3来讨论即可解答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、28g乙烯所含共用电子对数目为4NA |
| B、0.5mol 1,3-丁二烯分子中含有C=C双键数为NA |
| C、1 mol羟基所含的电子总数为10NA |
| D、标准状况下,11.2 L己烷所含分子数为0.5NA |
绿色化学己成为当前化学研究的热点和前沿,旨在从源头上消除污染,实现经济和社会可持续发展.而常温离子液体(ionic liquid)(也称常温熔融盐)以其优异的理化特性最有可能使上述理想变为现实.1914年报道的第一种离子液体硝酸乙基铵〔(C2H5NH3)NO3〕离子液体其熔点为12℃.已知C2H5NH2结合质子的能力比NH3略强,下列有关硝酸乙基铵的说法正确的是( )
| A、离子液体可以作为电池的电解质 |
| B、硝酸乙基铵水溶液呈碱性 |
| C、硝酸乙基铵水解的离子方程式表示为:C2H5NH3++H2O═C2H5NH2+H3O+ |
| D、相同温度下,相同物质的量浓度的硝酸乙基铵溶液和硝酸铵溶液前者的pH值小 |
高铁电池是一种新型可充电电池,电解质溶液为KOH,放电时的总反应式为:3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
| 放电 |
| 充电 |
| A、放电时负极反应为:3Zn+6e-+6OH-═3Zn(OH)2 |
| B、放电时OH-向负极移动 |
| C、充电时每转移3mol电子,阳极有1mol Fe(OH)3被还原 |
| D、充电时阴极反应式为:3Zn(OH)2+6e-+6H+═3Zn+6H2O |
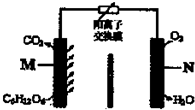 一种新型污水处理装置如图所示.该装置可利用一种微生物将有机废水的化学能直接转化为电能.下列说法中不正确的是( )
一种新型污水处理装置如图所示.该装置可利用一种微生物将有机废水的化学能直接转化为电能.下列说法中不正确的是( )| A、电池工作时H+从M极区移向N极区 |
| B、N极为正极,发生还原反应 |
| C、M极的电极反应式为:C6H12O6+6H2O-24e-═6CO2↑+24H+ |
| D、当N极消耗5.6L(标况下)气体时,则有2NA个H+通过离子交换膜 |
下列实验基本操作(或实验注意事项)中,主要是从实验安全角度考虑的是( )
| A、实验剩余的药品一般不能放回原试剂瓶 |
| B、溶解时用玻璃棒搅拌 |
| C、可燃性气体点燃前必须验纯 |
| D、过滤时玻璃棒靠在三层滤纸处 |