题目内容
如图所示的装置,X、Y都是惰性电极.将电源接通后,向(甲)中滴入酚酞溶液,在Fe 极附近显红色.试回答下列问题:

(1)三个装置中进行的化学反应,能量的转化形式是 ;
(2)乙装置的主要用途是 ;
(3)在电源中,B电极为 极(填电极名称,下同);丙装置中Y电极为 极;
(4)在甲装置中,石墨(C)电极上发生 反应(填“氧化”或“还原”);装置中总的化学方程式是: ;
(5)丙装置在通电一段时间后,Y电极上发生的电极反应式是 ;
(6)如果乙装置中精铜电极的质量增加了0.64g,请问甲装置中,铁电极上产生的气体在标准状况下为 升.

(1)三个装置中进行的化学反应,能量的转化形式是
(2)乙装置的主要用途是
(3)在电源中,B电极为
(4)在甲装置中,石墨(C)电极上发生
(5)丙装置在通电一段时间后,Y电极上发生的电极反应式是
(6)如果乙装置中精铜电极的质量增加了0.64g,请问甲装置中,铁电极上产生的气体在标准状况下为
考点:电解原理
专题:电化学专题
分析:(1)电解池是将电能转化为化学能的装置;
(2)根据电解精炼铜的原理来回答;
(3)电解饱和食盐水时,酚酞变红的极是阴极,阴极和电源负极相连,则在Fe极附近显红色,所以Fe是阴极,A是正极、B是负极,X是阳极,Y是阴极,
(4)根据电解池的工作原理以及电极反应来回答;
(5)在电解池的阴极上是电解质中的阳离子发生得电子的还原反应;
(6)根据串联电路中转移电子是相等的电子守恒规律来计算即可.
(2)根据电解精炼铜的原理来回答;
(3)电解饱和食盐水时,酚酞变红的极是阴极,阴极和电源负极相连,则在Fe极附近显红色,所以Fe是阴极,A是正极、B是负极,X是阳极,Y是阴极,
(4)根据电解池的工作原理以及电极反应来回答;
(5)在电解池的阴极上是电解质中的阳离子发生得电子的还原反应;
(6)根据串联电路中转移电子是相等的电子守恒规律来计算即可.
解答:
解:电解饱和食盐水时,酚酞变红的极是阴极,阴极和电源负极相连,则在Fe极附近显红色,所以Fe是阴极,A是正极、B是负极,X是阳极,Y是阴极
(1)该装置是电解池,电解池是将电能转化为化学能的装置,故答案为:将电能转化为化学能;
(2)乙装置中,粗铜和阳极相连,精铜和阴极相连,电解质是含有铜离子的盐溶液,所以是电解精炼铜的装置,故答案为:进行粗铜精炼;
(3)在Fe极附近显红色,所以Fe是阴极,A是正极、B是负极,X是阳极,Y是阴极,故答案为:负;阴,
(4)在甲装置中,石墨(C)电极是阳极,该电极上发生氧化反应,电解饱和食盐水的反应原理是:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,
故答案为:氧化;2NaCl+2H2O
2NaOH+H2↑+Cl2↑;
(5)在电解池的阴极上是电解质中的阳离子铜离子发生得电子的还原反应,即Cu2++2e-=Cu,故答案为:Cu2++2e-=Cu;
(6)乙装置中精铜电极的质量增加了0.64g,根据电极反应:Cu2++2e-=Cu,即生成0.64g即0.01mol铜,转移电子是0.02mol,铁电极是阴极,该极上产生氢气,2H++2e-=H2↑,当转移0.02mol电子时,该极上产生的气体为0.01mol,在标准状况下体积为0.224L,故答案为:0.224.
(1)该装置是电解池,电解池是将电能转化为化学能的装置,故答案为:将电能转化为化学能;
(2)乙装置中,粗铜和阳极相连,精铜和阴极相连,电解质是含有铜离子的盐溶液,所以是电解精炼铜的装置,故答案为:进行粗铜精炼;
(3)在Fe极附近显红色,所以Fe是阴极,A是正极、B是负极,X是阳极,Y是阴极,故答案为:负;阴,
(4)在甲装置中,石墨(C)电极是阳极,该电极上发生氧化反应,电解饱和食盐水的反应原理是:2NaCl+2H2O
| ||
故答案为:氧化;2NaCl+2H2O
| ||
(5)在电解池的阴极上是电解质中的阳离子铜离子发生得电子的还原反应,即Cu2++2e-=Cu,故答案为:Cu2++2e-=Cu;
(6)乙装置中精铜电极的质量增加了0.64g,根据电极反应:Cu2++2e-=Cu,即生成0.64g即0.01mol铜,转移电子是0.02mol,铁电极是阴极,该极上产生氢气,2H++2e-=H2↑,当转移0.02mol电子时,该极上产生的气体为0.01mol,在标准状况下体积为0.224L,故答案为:0.224.
点评:本题以电解池原理为载体考查了正负极的判断、电极反应式的书写等知识点,难度中等,明确溶液中离子的放电顺序是解本题的关键.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
核电荷数小于18的某元素X,其原子的电子层数n,最外层电子数为(2n+1),原子核内质子数为(2n2-1).下列关于元素X的说法中,不正确的是( )
| A、其最高化合价为+3价 |
| B、可以形成化学式为KXO3的盐 |
| C、其氢化物可以用来做喷泉实验 |
| D、其最高价氧化物的水化物是强酸 |
下列事故处理方法正确的是( )
| A、凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 |
| B、制取并用排水法收集氧气结束后,应立即停止加热 |
| C、浓NaOH溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 |
| D、浓硫酸溅到皮肤上,立即用稀NaOH溶液洗涤 |
能正确表示下列反应的离子方程式为( )
| A、硫化亚铁溶于稀硝酸中:FeS+2H+═Fe2++H2S↑ |
| B、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
| C、硫代硫酸钠溶液中滴入稀盐酸:S2O32-+2H+═S↓+SO2↑+H2O |
| D、在NaHSO4溶液中滴加Ba(OH)2至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
下列选用的相关仪器符合实验要求的是( )
A、 存放浓硝酸 |
B、 分离水和乙酸乙酯 |
C、 准确量取9.50mL水 |
D、 实验室制取乙烯 |
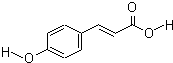 对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛.结构简式如图:
对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛.结构简式如图: