题目内容
11.能正确表示下列反应的离子方程式是( )| A. | 用过量氨水吸收工业尾气中的SO2:NH3•H2O+SO2═NH4++HSO3- | |
| B. | 氯化钠固体与浓硫酸混合加热:2H++H2SO4+2Cl-$\frac{\underline{\;△\;}}{\;}$SO2↑+Cl2↑+2H2O | |
| C. | 氧化亚铁溶于稀硝酸:3 Fe2++4H++NO3-═3Fe3++NO↑+2H2O | |
| D. | 0.01 mol•L-1 NH4Al(SO4)2溶液与0.02 mol•L-1Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O |
分析 A.氨水过量,反应生成亚硫酸铵和水;
B.浓硫酸与氯化钠固体反应生成硫酸钠和氯化氢气体,不会生成氯气;
C.氧化亚铁为氧化物,离子方程式中不能拆开;
D.铵根离子结合氢氧根离子能力大于氢氧化铝,氢氧化钡不足时生成氢氧化铝沉淀和一水合氨按.
解答 解:A.用过量氨水吸收工业尾气中的SO2,反应生成硫酸铵,正确得到离子方程式为:2NH3•H2O+SO2═2NH4++SO32-+2H2O,故A错误;
B.氯化钠固体与浓硫酸混合加热生成硫酸钠和氯气,正确的离子方程式为:H2SO4(浓)+2Cl-$\frac{\underline{\;△\;}}{\;}$SO42-+2HCl↑,故B错误;
C.氧化亚铁溶于稀硝酸反应生成硝酸铁、NO气体和水,正确的离子方程式为:3FeO+10H++NO3-═3Fe3++NO↑+5H2O,故C错误;
D.0.01 mol•L-1 NH4Al(SO4)2溶液与0.02 mol•L-1Ba(OH)2溶液等体积混合,反应生成硫酸钡沉淀、氢氧化铝沉淀和一水合氨按,反应的离子方程式为:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度中等,注意掌握明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
相关题目
6.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 25$°\\;C$C、101KPa下,NA个C18O2分子的质量为48g | |
| B. | 标准状况下,22.4L HF中含有的电子数为10NA | |
| C. | 1mol H3+O所含的电子数是11NA | |
| D. | 1L 0.1mol/L的NaClO水溶液中含有的氧原子数为0.1NA |
16.下列有关0.1mol•L-1 NaOH 溶液的叙述正确的是( )
| A. | 100mL该溶液中含有Na+0.01mol | |
| B. | 1 L该溶液中含有NaOH40 g | |
| C. | 从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01 mol•L-1 | |
| D. | 在1L水中溶解4g NaOH即可配制得0.1 mol•L-1 NaOH溶液 |
3.下列化合物中,同分异构体数目超过6个的有( )
| A. | 戊炔 | B. | 已烯 | C. | 1,2-二溴丙烷 | D. | 已烷 |
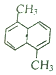 ,其苯环上的二溴代物有9种,苯环上的四溴代物有9种.
,其苯环上的二溴代物有9种,苯环上的四溴代物有9种.
 .
.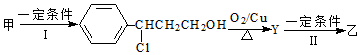
 ,设计步骤Ⅰ的目的是保护碳碳双键,防止被氧化.
,设计步骤Ⅰ的目的是保护碳碳双键,防止被氧化.