题目内容
20.配制250ml1mol•L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84g/ml,质量分数为98%)的体积为13.6ml.分析 依据C=$\frac{1000ρω}{M}$计算浓硫酸的物质的量浓度,依据溶液稀释过程中溶质的物质的量不变计算需要浓硫酸的体积,据此解答.
解答 解:密度为1.84g/ml,质量分数为98%物质的量浓度C=$\frac{1000×1.84×98%}{98}$=18.4mol/L,设配制250ml1mol•L-1的稀H2SO4溶液,需要浓硫酸体积为V,则依据溶液稀释过程中溶质的物质的量不变得:18.4mol/L×V=250ml×1mol•L-1,解得V=13.6mL,
故答案为:13.6.
点评 本题考查了一定物质的量浓度溶液的配制,侧重考查有关物质的量计算,明确溶液稀释过程中溶质的物质的量不变是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.能正确表示下列反应的离子方程式是( )
| A. | 用过量氨水吸收工业尾气中的SO2:NH3•H2O+SO2═NH4++HSO3- | |
| B. | 氯化钠固体与浓硫酸混合加热:2H++H2SO4+2Cl-$\frac{\underline{\;△\;}}{\;}$SO2↑+Cl2↑+2H2O | |
| C. | 氧化亚铁溶于稀硝酸:3 Fe2++4H++NO3-═3Fe3++NO↑+2H2O | |
| D. | 0.01 mol•L-1 NH4Al(SO4)2溶液与0.02 mol•L-1Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O |
15.在有机物分子结构的鉴定中常用核磁共振氢谱分析法来测定有机化合物分子( )
| A. | 相对分子质量 | B. | 氢原子在碳骨架上的位置和数目 | ||
| C. | 含有何种化学键或官能团 | D. | 键长、键角及分子的三维结构 |
9.已知平衡:①C2H4(g)?C2H2(g)+H2(g),②2CH4(g)?C2H4(g)+2H2(g).当温度升高时,①和②式均向右移动.
a.C(s)+2H2(g)═CH4(g)△H1; b.2C(s)+H2(g)═C2H2(g)△H2;
c.2C(s)+2H2(g)═C2H4(g)△H3;
下列有关a、b和c中△H1、△H2、△H3的大小顺序排列正确的是( )
a.C(s)+2H2(g)═CH4(g)△H1; b.2C(s)+H2(g)═C2H2(g)△H2;
c.2C(s)+2H2(g)═C2H4(g)△H3;
下列有关a、b和c中△H1、△H2、△H3的大小顺序排列正确的是( )
| A. | △H1>△H2>△H3 | B. | △H2>△H3>△H1 | C. | △H2>△H1>△H3 | D. | △H3>△H2>△H1 |
10.下列关于氮及其化合物的说法正确的是( )
| A. | N2分子的结构稳定,因而氮气不能支持任何物质的燃烧 | |
| B. | 液氨汽化时要吸收大量热,因而液氨可用作制冷剂 | |
| C. | NO可用向上排空气法或者排水法收集 | |
| D. | 浓硝酸保存在棕色瓶内是因为硝酸易挥发 |
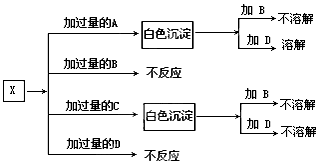 A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种.现利用另一种溶液X,用如下图所示的方法即可将它们确定.
A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种.现利用另一种溶液X,用如下图所示的方法即可将它们确定.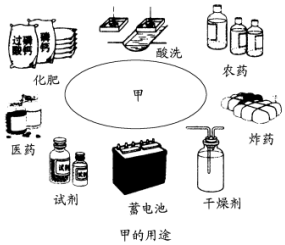 a、b、c是原子序数依次增大的三种常见短周期元素.由a、b、c三元素组成的化合物甲的用途如下图所示.a、b、c三元素之间两两化合可生成化合物乙、丙、丁、戊4种.化合物甲、乙、丙、丁、戊之间也能相互反应.已知乙、戊分别是由a、b两元素按原子个数1:1和2:1组成的化合物.若a、b、c三元素形成的单质(仍用a、b、c表示)和由它们组成的化合物之间的反应关系如下(未配平)
a、b、c是原子序数依次增大的三种常见短周期元素.由a、b、c三元素组成的化合物甲的用途如下图所示.a、b、c三元素之间两两化合可生成化合物乙、丙、丁、戊4种.化合物甲、乙、丙、丁、戊之间也能相互反应.已知乙、戊分别是由a、b两元素按原子个数1:1和2:1组成的化合物.若a、b、c三元素形成的单质(仍用a、b、c表示)和由它们组成的化合物之间的反应关系如下(未配平)