题目内容
已知乙醇密度小于水,质量分数为96%的酒精溶液的物质的量浓度为16.6mol?L-1,试判断8.3mol?L-1的酒精溶液的溶质的质量分数为( )
| A、大于48% | B、等于48% |
| C、小于48% | D、无法确定 |
考点:溶液中溶质的质量分数及相关计算
专题:
分析:设物质的量浓度为16.6mol?L-1的溶液的密度为Dg/mL,浓度为8.3mol?L-1的酒精溶液的密度为d g/mL,溶质的质量分数为w,根据c=
表示出物质的量浓度,进而表示出w,而酒精的密度小于水,溶液浓度越大,密度越小,则D<d,据此计算判断.
| 1000ρω |
| M |
解答:
解:设物质的量浓度为16.6mol?L-1的溶液的密度为Dg/mL,浓度为8.3mol?L-1的酒精溶液的密度为d g/mL,溶质的质量分数为w.
则:16.6=
,8.3=
,
故w=
,酒精的密度小于水,溶液浓度越大,密度越小,则D<d,故w<48%
故选C.
则:16.6=
| 1000D×96% |
| 46 |
| 1000d×w |
| 46 |
故w=
| 48%D |
| d |
故选C.
点评:本题考查物质的量浓度的计算,题目难度中等,注意酒精的密度小于水,溶液浓度越大,密度越小,理解掌握物质的量浓度越质量分数之间的关系.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4
2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法正确的是( )
| ||
| A、KClO3在反应中得到电子 |
| B、H2SO4是该反应的氧化剂 |
| C、H2C2O4在反应中被还原 |
| D、1 mol KClO3参加反应,有2mol电子转移 |
下列电离方程式正确的是( )
A、
| ||||
| B、Ba(OH)2?Ba2++2OH- | ||||
| C、HCO3-+H2O?H2O++CO32- | ||||
| D、NaHCO3?Na++H++CO32- |
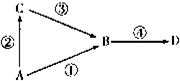 A、B、C、D均为中学常见物质,其中A为单质,B、C、D为化台物,并且存在如下转化关系:试回答下列问题:
A、B、C、D均为中学常见物质,其中A为单质,B、C、D为化台物,并且存在如下转化关系:试回答下列问题: