题目内容
下列电离方程式正确的是( )
A、
| ||||
| B、Ba(OH)2?Ba2++2OH- | ||||
| C、HCO3-+H2O?H2O++CO32- | ||||
| D、NaHCO3?Na++H++CO32- |
考点:电离方程式的书写
专题:电离平衡与溶液的pH专题
分析:强电解质完全电离,用等号,弱电解质部分电离,用可逆号,多元弱酸分步电离,原子团不能拆.
解答:
解:A.乙二酸为多元弱酸分步电离,电离方程式为: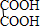

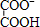 +H+,
+H+,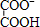

+H+,故A错误;
B.氢氧化钡为强电解质,完全电离用等号,电离方程式:Ba(OH)2=Ba2++2OH-,故B错误;
C.碳酸氢根离子为多元弱酸的酸式根离子,电离生成氢离子和碳酸根离子,电离方程式:HCO3-+H2O?H2O++CO32-,故C正确;
D.碳酸氢根离子为多元弱酸的酸式根离子,不能拆,电离方程式为:NaHCO3=Na++HCO3-,故D错误;
故选:C.
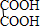

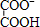 +H+,
+H+,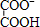

COO- COO- |
B.氢氧化钡为强电解质,完全电离用等号,电离方程式:Ba(OH)2=Ba2++2OH-,故B错误;
C.碳酸氢根离子为多元弱酸的酸式根离子,电离生成氢离子和碳酸根离子,电离方程式:HCO3-+H2O?H2O++CO32-,故C正确;
D.碳酸氢根离子为多元弱酸的酸式根离子,不能拆,电离方程式为:NaHCO3=Na++HCO3-,故D错误;
故选:C.
点评:本题考查了电解质电离方程式的书写,明确电解质的强弱和电离方式是解题关键,注意多元酸弱酸分步电离,碳酸氢根离子不能拆.

练习册系列答案
相关题目
下列关于煤的综合利用的说法正确的是( )
| A、煤中含有苯、甲苯、二甲苯等有机物 |
| B、煤的气化、液化和干馏是煤综合利用的主要方法 |
| C、煤的气化液化是物理变化 |
| D、煤的干馏和石油的分馏均为物理变化 |
已知乙醇密度小于水,质量分数为96%的酒精溶液的物质的量浓度为16.6mol?L-1,试判断8.3mol?L-1的酒精溶液的溶质的质量分数为( )
| A、大于48% | B、等于48% |
| C、小于48% | D、无法确定 |
1mol O2在放电条件下发生下列反应:3O2
2O3,如有30%O2转化为O3,则放电后混合气体对H2的相对密度是( )
| ||
| A、17.8 | B、16 |
| C、18.4 | D、35.6 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温下,23g NO2含有NA个氧原子 | ||
| B、0.1mol?L-1的烧碱溶液中含有0.1NA个Na + | ||
| C、22.4 L的CO气体与1 mol N2所含的分子数相等 | ||
D、9 g
|
下列离子方程式,书写正确的是( )
| A、硝酸银溶液中加入铜粉 Ag++Cu═Cu2++Ag↓ |
| B、氯化铁溶液中加入过量氨水 Fe3++3OH-=Fe(OH)3↓ |
| C、铝粉投入到NaOH溶液中 2Al+2OH-═2AlO2-+H2↑ |
| D、硫酸铜溶液中滴加氢氧化钡溶液 Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓ |
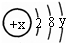 试回答:
试回答: