题目内容
9.氯化亚铜(CuCl)是一种精细化工产品,常用作催化剂,还可用于颜料、防腐等工业.难溶于水和乙醇,可溶于氯离子浓度较大的体系中形成络合离子[CuCl2]-,且存在[CuCl2]-?CuCl↓+Cl-.在潮湿的空气中易被氧化,热水中可水解.某课题组拟制备氯化亚铜,甲设计方案如下:
(一)制备氯化铜(CuCl2)(图)
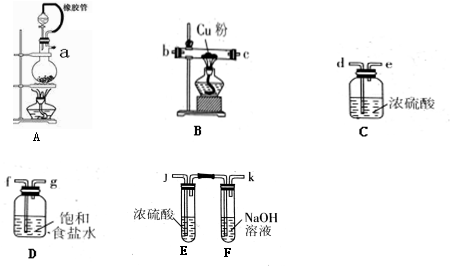
(1)实验室常用MnO2和浓盐酸反应制氯气,化学反应方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.制备氯化铜,从左到右接口的连接顺序是:a→f、g、d、e、b(c)、c(b)(填字母代号).A装置中橡胶管的作用平衡气压,有利浓盐酸滴加.
(2)遵循简约性原则,F、G装置可以用一个装置替代(写出名称、盛装的试剂)装碱石灰的干燥管.
(二)制备氯化亚铜
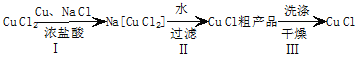
(3)步骤Ⅰ的化学方程式为:CuCl2+Cu+2NaCl=2Na[CuCl2];步骤Ⅱ加水的目的是降低氯离子浓度促使氯化亚铜析出.
乙设计方案如:采用亚硫酸盐还原法,利用电镀废液制备氯化亚铜
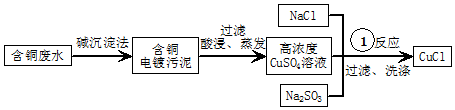
(4)反应①制备氯化亚铜的离子反应方程式为H2O+SO32-+2Cu2++2Cl-=2CuCl↓+SO42-+2H+.
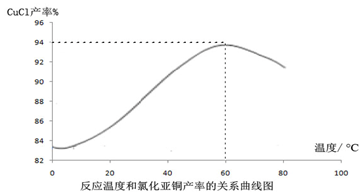
如图,溶液温度控制在60℃左右时,CuCl产率可达到94%,随后随温度升高CuCl产率会下降,其原因是温度进一步升高CuCl的水解程度增大进而造成CuCl产率降低或温度高于60℃CuCl水解显著进而造成CuCl产率降低.
分析 (一)制备氯化铜(CuCl2):A装置用二氧化锰和和浓盐酸制备氯气,制备的氯气中混有氯化氢和水蒸气,由饱和食盐水吸收氯化氢气体,由浓硫酸吸收水蒸气,为除杂充分,导气管均长进短出,纯净干燥的氯气与铜粉在玻璃管中反应制备氯化铜,据此分析;
(二)制备氯化亚铜:
(3)将氯化铜与铜、氯化钠混合,发生反应CuCl2+Cu+2NaCl=2Na[CuCl2],有[CuCl2]-?CuCl↓+Cl-,加水促进该平衡正向移动,生成氯化亚铜;
(4)根据流程,氯化钠、高浓度的硫酸铜溶液、亚硫酸钠混合反应生成氯化亚铜,铜元素化合价降低,被亚硫酸根离子还原,则亚硫酸根离子被氧化为硫酸根离子,据此书写;由题可知,氯化亚铜热水中可水解,根据温度对水解平衡的影响分析.
解答 解:(1)实验室常用MnO2和浓盐酸反应制氯气,MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;氯气(混有氯化氢、水蒸气)由a经过饱和食盐水、浓硫酸除杂,导气管长进短出,最后与铜粉反应,则连接f、g、d、e、b(c)、c(b);A装置中橡胶管的作用平衡气压,有利浓盐酸滴加;
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;f、g、d、e、b(c)、c(b);平衡气压,有利浓盐酸滴加;
(2)碱石灰既能吸收水蒸气由能吸收酸性气体,故可由装碱石灰的干燥管代替;
故答案为:装碱石灰的干燥管;
(3)将氯化铜与铜、氯化钠混合,反应为:CuCl2+Cu+2NaCl=2Na[CuCl2];存在[CuCl2]-?CuCl↓+Cl-,加入水,降低氯离子浓度促使氯化亚铜析出;
故答案为:CuCl2+Cu+2NaCl=2Na[CuCl2];降低氯离子浓度促使氯化亚铜析出;
(4)根据流程,氯化钠、高浓度的硫酸铜溶液、亚硫酸钠混合反应生成氯化亚铜,铜元素化合价降低,被亚硫酸根离子还原,则亚硫酸根离子被氧化为硫酸根离子,离子方程式为:H2O+SO32-+2Cu2++2Cl-=2CuCl↓+SO42-+2H+;由题可知,氯化亚铜热水中可水解,温度进一步升高CuCl的水解程度增大进而造成CuCl产率降低或温度高于60℃CuCl水解显著进而造成CuCl产率降低;
故答案为:H2O+SO32-+2Cu2++2Cl-=2CuCl↓+SO42-+2H+;温度进一步升高CuCl的水解程度增大进而造成CuCl产率降低或温度高于60℃CuCl水解显著进而造成CuCl产率降低.
点评 本题考查性质实验方案设计,侧重考查学生知识综合应用、根据实验目的及物质的性质进行排列顺、氧化还原反应、水解平衡等,综合性较强,注意把握物质性质以及对题目信息的获取于使用,难度中等.

 备战中考寒假系列答案
备战中考寒假系列答案| A. | 用规格为10 mL的量筒量取6mL的液体 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
 雾霾天气严重影响人们的生活和健康.其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等.因此改善能源结构、机动车限号等措施能有效减少PM2.5、SO2、NOx等污染.
雾霾天气严重影响人们的生活和健康.其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等.因此改善能源结构、机动车限号等措施能有效减少PM2.5、SO2、NOx等污染.请回答下列问题:
(1)将一定量的某利M2.5样品用蒸馏水溶解制成待测试样(忽略OH-).常温下测得该训试样的组成及其浓度如表一:根据表一中数据判断该试样的pH=4.
表一:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度mol/L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
A.混合气体的密度不再变化 B.混合气体的压强不再变化
C.N2、O2、NO的物质的量之比为1:1:2D.氧气的转化率不再变化
(3)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料.已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8KJ•mol-1
C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5KJ•mol-1
写出焦炭与水蒸气反应的热化学方程式:C(s)+H2O(g)═CO(g)+H2(g)△H=+13l.3kJ•mol-1.
②洗涤含SO2的烟气.下列可作为洗涤含SO2的烟气的洗涤剂的是AB.
A.浓氨水 B.碳酸氢钠饱和溶液 C.FeCl2饱和溶液 D.酸性CaCl2饱和溶液
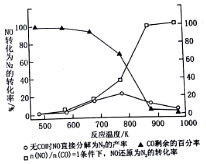
(4)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.某研究性小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示.若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因为NO的分解反应是放热反应,升温有利于反应逆向进行,在$\frac{n(NO)}{n(CO)}$=1的条件下,为更好的除去NOx物质,应控制的最佳温度在870K左右.
(5)车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如表二:
表二:
| 物质 温度/℃ | 活性炭 | NO | E | F |
| 初始 | 3.000 | 0.10 | 0 | 0 |
| T1 | 2.960 | 0.020 | 0.040 | 0.040 |
| T2 | 2.975 | 0.050 | 0.025 | 0.025 |
③上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为80%.
| A. | 铝及其合金是生活中广泛使用的材料,通常用电解氯化铝的方法制取 | |
| B. | 采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量 | |
| C. | 偏二甲肼[NH2N(CH3)2]是一种液体燃料,它的一种同分异构体可以是氨基酸 | |
| D. | 邻苯二甲酸二辛酯常用作增塑剂,对人体无害,可用作食品添加剂 |
| A. | 1mol蔗糖完全水解生成葡萄糖分子数为2 NA | |
| B. | 在氢氧碱性燃料电池中,若正极消耗22.4L气体(标准状况),则转移电子数为2NA | |
| C. | 16.0 gCuO和Cu2S的混合物含阴离子数为0.2NA | |
| D. | 2.24L(标准状况)一氯甲烷分子中含共价键数为0.4NA |
| A. | 单质的沸点:Y>W>Z | B. | 离子半径:X<Y | ||
| C. | 气态氢化物的稳定性:W>Y | D. | W与X可形成离子化合物 |
CH2=CH-COOH+H2O$\stackrel{一定条件}{→}$
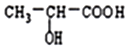
| A. | 该反应为加成反应,没有副产物生成 | |
| B. | 可用Br2/CCl4溶液鉴别丙烯酸和乳酸 | |
| C. | 丙烯酸与乳酸都属于有机酸,两者不发生反应 | |
| D. | 1mol乳酸分别与足量Na、NaOH、NaHCO3反应,消耗三者物质的量之比为2:2:1 |