题目内容
在核电荷数为26的元素Fe的原子核外的3d、4s轨道内,下列电子排布图正确的是( )
A、 |
B、 |
C、 |
D、 |
考点:原子核外电子排布
专题:
分析:能量最低原理:原子核外电子先占有能量较低的轨道.然后依次进入能量较高的轨道.
保里不相容原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子.
洪特规则:原子核外电子在能量相同的各个轨道上排布时①电子尽可能分占不同的原子轨道,②自旋状态相同,③特例:全空、全满或半满时能量最低.
保里不相容原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子.
洪特规则:原子核外电子在能量相同的各个轨道上排布时①电子尽可能分占不同的原子轨道,②自旋状态相同,③特例:全空、全满或半满时能量最低.
解答:
解:根据能量最低原理、保里不相容原理、洪特规则知,Fe原子3d能级上有6个电子,4s能级上有2个电子,该原子最稳定、能量最低,因此价电子排布图为 ,
,
A、违反了能量最低原理,故A错误;
B、违反了能量最低原理,故B错误;
C、违反了洪特规则,故C错误;
D、3d能级上有6个电子,4s能级上有2个电子,该原子最稳定、能量最低,故D正确;
故选D.
 ,
,A、违反了能量最低原理,故A错误;
B、违反了能量最低原理,故B错误;
C、违反了洪特规则,故C错误;
D、3d能级上有6个电子,4s能级上有2个电子,该原子最稳定、能量最低,故D正确;
故选D.
点评:本题考查了原子核外电子排布,根据能量最低原理、保里不相容原理、洪特规则来分析解答即可,难度不大.

练习册系列答案
相关题目
下列各项中离子方程式的书写与反应物的用量无关的是( )
| A、AlCl3溶液与稀氨水 |
| B、FeBr2溶液与Cl2 |
| C、CO2与Na2SiO3溶液 |
| D、澄清石灰水与Ca(HCO3)2溶液 |
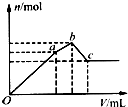 向100mL0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1Ba(OH)2溶液.随着Ba(OH)2溶液体积(V)的变化,沉淀总物质的量(n)的变化如图所示.下列叙述正确的是( )
向100mL0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1Ba(OH)2溶液.随着Ba(OH)2溶液体积(V)的变化,沉淀总物质的量(n)的变化如图所示.下列叙述正确的是( )| A、a点的沉淀总物质的量为0.03mol |
| B、Oa段发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-═Al(OH)3↓+2BaSO4↓ |
| C、ab段发生反应的离子方程式是:2NH42++SO42-+Ba2++2OH-═2NH3?H2O+BaSO4↓ |
| D、反应到c点时,加入Ba(OH)2溶液的总体积为250mL |
下列有关物质的性质与应用相对应的是( )
| A、稀硝酸具有氧化性,可用于清洗做银镜反应的试管 |
| B、BaSO4、BaCO3均难溶于水,都可用作钡餐 |
| C、铝合金的大量使用归功于人们能用焦炭等还原剂从氧化铝中获取铝 |
| D、加热盛有NH4Cl固体的试管,管口有固体凝结,这是升华现象 |
下列物质混合后,不能发生离子反应的是( )
| A、Na2CO3溶液与稀盐酸 |
| B、CuSO4溶液与BaCl2溶液 |
| C、稀H2SO4与NaCl溶液 |
| D、稀HNO3与Ba(OH)2溶液 |
下列物质属于非电解质的是( )
| A、醋酸 | B、氯化钠 |
| C、氢氧化钠 | D、酒精 |