题目内容
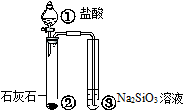
碳酸氢钠与盐酸反应 .
考点:钠的重要化合物
专题:元素及其化合物
分析:碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳.
解答:
解:碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳,反应的方程式为HCl+NaHCO3=NaCl+H2O+CO2↑,故答案为:HCl+NaHCO3=NaCl+H2O+CO2↑.
点评:本题考查碳酸氢钠的性质,为高频考点,注意碳酸氢钠与酸、碱反应的特点以及相关方程式的书写,题目侧重基础,难度不大.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
向一定量的Fe、FeO、Fe2O3的混合物中加入100ml浓度为1mol/L的硫酸,恰好使混合物完全溶解,放出标况下224ml的气体.所得溶液中加入KSCN溶液后无血红色出现.若用足量的H2在高温下还原相同质量的此混合物,能得到铁的质量是( )
| A、11.2g | B、5.6g |
| C、2.8g | D、1.4g |
将10g具有1个羟基的化合物A跟乙酸在一定条件下反应,生成某酯17.6g,并回收了未反应的A 0.8g.则化合物A的相对分子质量为( )
| A、146 | B、114 |
| C、92 | D、46 |
一定条件下,容积为2L的恒容密闭容器中,通入2mol N2、3mol H2进行反应催化剂高温高压N2(g)+3H2(g)?2NH3(g),20min后,N2的物质的量为1.9mol,1h后测得容器内气体的压强不再改变,且为反应开始时压强的0.8倍,则下列叙述正确的是( )
| A、1 h后反应进行完全,容器中的N2浓度为0.55 mol?L-1 |
| B、前20 min用NH3表示的反应速率为0.01 mol?L-1?min-1 |
| C、增加H2的浓度或降低温度,平衡将向正反应方向移动,且反应速率均加快 |
| D、当容器内压强不改变时,说明反应已达到平衡状态 |
科学家相信,第七周期包含的元素数目与第六周期相同,若118号元素将来被确认,则下列预测合理的是( )
| A、它的中子数是118 |
| B、它是第八周期元素 |
| C、它是活泼的金属元素 |
| D、它的最外层电子数是8 |
有关如图装置的叙述正确的是( )


| A、这是一个电解池装置 |
| B、这是电解NaOH溶液的装置 |
| C、该装置中Fe为阴极,电极反应为:Fe-2e-+2OH-=Fe(OH)2 |
| D、该装置中Pt为正极,电极反应为:O2+2H2O+4e-=4OH- |
下列物质的水溶液中只存在一种分子的是( )
| A、NaF |
| B、HNO3 |
| C、NaHS |
| D、HClO |