题目内容
14.根据原子结构、元素周期表和元素周期律的知识回答下列问题:(1)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是铬,在元素周期表中的位置是第四周期第ⅥB族.
(2)C元素基态原子的电子排布图是如图中的②(填序号),另一电子排布图不能作为基态原子的电子排布图是因为它不符合C(从A B C中选择).
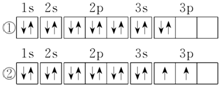
A.能量最低原理 B.泡利原理 C.洪特规则
(3)依据正负化合价代数和等于0,H元素可以放在周期表中的ⅣA族.
(4)氯化铵的电子式
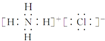 .
.
分析 (1)1~36号元素,未成对电子数最多的元素外围电子排布为3d54s1,共有6个未成对电子;
(2)由电子排布图中的电子数知,C元素是硅,根据洪特规则,当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,且自旋方向相同;
(3)正负化合价代数和等于0,说明正负化合价的绝对值相等,都是4,据此判断H所在族;
(4)氯化铵为离子化合物,阴阳离子都需要标出所带电荷及最外层电子,据此形成氯化铵的电子式.
解答 解:(1)1~36号元素,未成对电子数最多的元素外围电子排布为3d54s1,共有6个未成对电子,该元素是铬,处于周期表中第四周期第ⅥB族,
故答案为:铬;第四周期第ⅥB族;
(2)由电子排布图中的电子数知,C元素是硅,根据洪特规则,当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,且自旋方向相同,故硅元素基态原子的电子排布图为②,
故答案为:②;C;
(3)正负化合价代数和等于0,说明该元素最外层含有4个电子,则H元素可以放在周期表中ⅣA,
故答案为:ⅣA;
(4)氯化铵为离子化合物,铵根离子和钠离子都需要标出所带电荷及最外层电子,氯化铵的电子式为: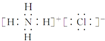 ,
,
故答案为: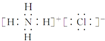 .
.
点评 本题考查了原子结构与元素周期律的应用,题目难度中等,明确原子结构与元素周期律、元素周期表的关系为解答关键,试题侧重基础知识的考查,有利于提高学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
3.黑火药爆炸的反应为:2KNO3+3C+S═K2S+N2↑+3CO2↑,则被氧化的元素是( )
| A. | 碳和氢 | B. | 氮和硫 | C. | 只有硫 | D. | 只有碳 |
4.已知:2NaAlO2+CO2+3H2O=2A1(OH)3↓+Na2CO3,向含2molNaOH、1molBa(OH)2、2molNaAlO2的混合溶液中慢慢通人CO2,则通人CO2的量和生成沉淀的量的关系正确的是( )
| 选项 | A | B | C | D |
| n(CO2)/mol | 2 | 3 | 4 | 5 |
| n(沉淀)/mol | 2 | 2 | 3 | 2 |
| A. | A | B. | B | C. | C | D. | D |
2.在密闭容器中把CO和H2O的混合物加热到800℃,有下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g),且平衡常数K=1.若在2L的密闭容器中充入1mol CO和1mol H2O相互混合并加热到800℃,则CO的转化率为( )
| A. | 40% | B. | 50% | C. | 60% | D. | 83.3% |
9.常温下,用0.1000mol•L-1NaOH溶液滴定20.00mL 0.1000mol•L-1CH3 COOH溶液所得滴定曲线如图.下列说法正确的是( )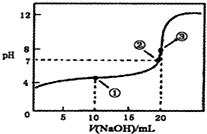

| A. | ①处水的电离程度大于②处水的电离程度 | |
| B. | ②处加入的NaOH溶液恰好将CH3COOH中和 | |
| C. | ③处所示溶液:c(N+)<c(CH3COO-) | |
| D. | 滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
19.元素X与元素Y在周期表中位于相邻的两个周期,X与Y两原子核外电子数之和为19,Y原子核内质子数比X多3个.下列描述正确的是( )
| A. | X和Y都是性质活泼的元素,在自然界中只能以化合态存在 | |
| B. | X和Y形成的化合物的化学式只能为Y2X2 | |
| C. | X的化合物种类比Y的化合物种类多 | |
| D. | Y能置换酸中氢放出氢气,但不能置换盐中的金属 |
6.1mol某烃能与2mol HCl完全加成,其产物最多能被8mol Cl2完全取代,则原烃可为( )
| A. | 乙炔 | B. | 1-丁炔 | C. | 1-丙炔 | D. | 环丁烯 |
3.下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 含大量Fe3+的溶液中:Na+、Mg2+、SO42-、SCN- | |
| B. | 使甲基橙呈红色的溶液:NO3-、Ba2+、AlO2-、Cl- | |
| C. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- | |
| D. | pH=12的溶液:CO32-、Cl-、K+、F- |
4.微型纽扣电池在现代生活中是广泛应用的一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电池总反应式为Ag2O+Zn═2Ag+ZnO.根据上述反应式,判断下列叙述中正确的是( )
| A. | 在使用过程中,电池负极区溶液pH增大 | |
| B. | 在使用过程中,电子由Ag2O极经外电路流向Zn极 | |
| C. | 在使用过程中,Zn电极发生还原反应,Ag2O电极发生氧化反应 | |
| D. | 外电路中每通过0.2 mol电子,正极的质量理论上减小1.6 g |