题目内容
2.在密闭容器中把CO和H2O的混合物加热到800℃,有下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g),且平衡常数K=1.若在2L的密闭容器中充入1mol CO和1mol H2O相互混合并加热到800℃,则CO的转化率为( )| A. | 40% | B. | 50% | C. | 60% | D. | 83.3% |
分析 依据化学平衡的三段式列式计算,结合平衡常数表达式计算消耗的一氧化碳的物质的量,结合转化率概念计算得到,反应前后气体物质的量不变,可以利用气体物质的量代替平衡浓度计算平衡常数.
解答 解:在密闭容器中将CO和水蒸气的混合物加热到800℃时,达到平衡状态,设消耗一氧化碳物质的量为x:
CO+H2O?CO2+H2,
起始量(mol) 2 1 0 0
变化量(mol) x x x x
平衡量(mol)1-x 1-x x x
反应前后气体物质的量不变,可以利用气体物质的量代替平衡浓度计算平衡常数,
平衡常数K=$\frac{x×x}{(1-x)×(1-x)}$=1,
解得:x=0.5mol
则CO的转化率=$\frac{0.5mol}{1mol}$×100%=50%,
故选B.
点评 本题考查了化学平衡的计算,题目难度不大,明确化学平衡常数的概念及表达式为解答关键,注意掌握三段式在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
11.下列化合物不能由两种单质直接化合而生成的是( )
| A. | Fe2S3 | B. | Na2S | C. | Cu2S | D. | FeCl3 |
12.下列事实对应的离子方程式或电极反应式书写正确的是( )
| A. | 用石墨作电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+4H+ | |
| B. | 碳酸钠溶液显碱性:CO32-+2H2O?H2CO3+2OH- | |
| C. | 钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-═Fe3+ | |
| D. | NaHSO4在水溶液中电离:NaHSO4=Na++HSO4- |
9.常温下,向25mL 0.1mol•L-1弱碱MOH溶液中逐滴滴加0.2mol•L-1的HCl,溶液pH的变化曲线如图所示(溶液混合时体积的变化忽略不计).下列说法正确的是( )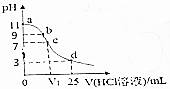

| A. | MOH电离方程式为:MOH═M++OH- | |
| B. | 在b点,离子浓度大小为c(OH-)>c(H+)>c(M+)>c(Cl-) | |
| C. | 在c点,滴加的V(HCl)>12.5mL | |
| D. | 在d点,c(Cl-)=2c(MOH)+2c(M+)=0.1mol•L-1 |
7.下列说法正确的是( )
| A. | 向稀的Na2CO3和NaHCO3溶液中加入CaCl2溶液均有白色沉淀产生 | |
| B. | 向Al2(SO4)3溶液中逐滴滴入NaOH溶液与向NaOH溶液中逐滴滴入Al2(SO4)3溶液,产生的现象相同 | |
| C. | 等质量的Al分别与过量的NaOH、HCl溶液反应,NaOH溶液中放出的H2多 | |
| D. | 分别向Na2CO3和NaHCO3溶液中滴加澄清石灰水,都能生成白色沉淀 |
11.下列关于硅的化学性质的叙述,正确的是( )
| A. | 常温时不和任何酸反应 | B. | 常温时可和强碱溶液反应 | ||
| C. | 单质硅比碳的还原性弱 | D. | 单质硅比碳的氧化性强 |
12.用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,11.2 L SO3所含的原子数为2NA | |
| B. | 标准状况下,22.4L氧气和乙炔混合物所含的分子数为NA | |
| C. | 0.2 mol过氧化氢完全分解转移的电子数目为0.4 NA | |
| D. | 46g NO2和N2O4的混合物所含的分子数为NA |
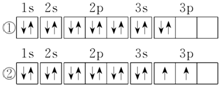
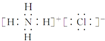 .
.