题目内容
(宏志班做)
在一定条件下,在容积为2L的密闭容器中,将2mol气体M和3mol气体N混合,发生如下反应:2M(g)+3N(g)?x Q(g)+3R(g),经2min达平衡,生成2.4molR,并测得Q的浓度为0.4mol/L.求:
(1)用气体M来表示该反应的化学反应速率是多少?
(2)反应前后的压强比?
(3)N的转化率是多少?
(4)平衡时气体Q所占的体积分数为多少?
在一定条件下,在容积为2L的密闭容器中,将2mol气体M和3mol气体N混合,发生如下反应:2M(g)+3N(g)?x Q(g)+3R(g),经2min达平衡,生成2.4molR,并测得Q的浓度为0.4mol/L.求:
(1)用气体M来表示该反应的化学反应速率是多少?
(2)反应前后的压强比?
(3)N的转化率是多少?
(4)平衡时气体Q所占的体积分数为多少?
考点:化学平衡的计算
专题:化学平衡专题
分析:结合化学平衡三段式列式计算,根据n=cV计算生成Q的物质的量,结合R的物质的量,利用物质的量之比等于化学计量数之比计算x的值;
(1)依据反应速率V=
计算得到;
(2)反应前后气体压强之比等于气体物质的量之比;
(3)根据C可知参加反应N的物质的量,N的转化率=
×100%;
(4)平衡时气体Q所占的体积分数,可以利用气体物质的量分数计算.
(1)依据反应速率V=
| △c |
| △t |
(2)反应前后气体压强之比等于气体物质的量之比;
(3)根据C可知参加反应N的物质的量,N的转化率=
| 参加反应的N的物质的量 |
| N的起始物质的量 |
(4)平衡时气体Q所占的体积分数,可以利用气体物质的量分数计算.
解答:
解:经2min达平衡,生成2.4molR,并测得Q的浓度为0.4mol/L,Q物质的量=0.4mol/L×2L=0.8mol,物质的量之比等于化学计量数之比,0.8:2.4=x:3,计算得到x=1;
2M(g)+3N(g)?Q(g)+3R(g)
起始量(mol) 2 3 0 0
变化量(mol) 1.6 2.4 0.8 2.4
平衡量(mol) 0.4 0.6 0.8 2.4
(1)用气体M来表示该反应的化学反应速率=
=0.4mol/L;
答:用气体M来表示该反应的化学反应速率0.4mol/L;
(2)反应前后的压强比=气体物质的量之比=(2+3):(0.4+0.6+0.8+2.4)=25:21;
答:反应前后的压强比25:21;
(3)N的转化率=
×100%=80%;
答:N的转化率80%;
(4)平衡时气体Q所占的体积分数=气体物质的量分数=
×100%=19%;
答:平衡时气体Q所占的体积分数19%.
2M(g)+3N(g)?Q(g)+3R(g)
起始量(mol) 2 3 0 0
变化量(mol) 1.6 2.4 0.8 2.4
平衡量(mol) 0.4 0.6 0.8 2.4
(1)用气体M来表示该反应的化学反应速率=
| ||
| 2min |
答:用气体M来表示该反应的化学反应速率0.4mol/L;
(2)反应前后的压强比=气体物质的量之比=(2+3):(0.4+0.6+0.8+2.4)=25:21;
答:反应前后的压强比25:21;
(3)N的转化率=
| 2.4mol |
| 3mol |
答:N的转化率80%;
(4)平衡时气体Q所占的体积分数=气体物质的量分数=
| 0.8mol |
| 0.4mol+0.6mol+0.8mol+2.4mol |
答:平衡时气体Q所占的体积分数19%.
点评:本题考查了化学平衡计算分析应用,主要是气体体积分数,转化率,压强之比等的计算应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
有下列原子:
Li、
Li、
Na、
Mg、
C、
N,关于这些原子的说法中正确的是( )
6 3 |
7 3 |
23 11 |
24 12 |
14 6 |
14 7 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
已知R2+离子核外有a个电子,b个中子,表示R原子符号正确的是( )
A、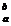 R R |
B、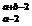 R R |
C、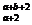 R R |
D、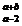 R R |
下列离子方程式书写正确的是( )
| A、碳酸氢钙溶液中加入少量的氢氧化钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| B、硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ |
| C、钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
| D、NaOH溶液中通入过量SO2:2OH-+SO2═SO32-+H2O |
NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol甲基(-14C1H3)所含的中子数和电子数分别为8NA、9NA |
| B、标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA |
| C、标准状况下,2.24L Cl2全部被NaOH溶液吸收,转移的电子数目为0.2NA |
| D、在高温、高压、催化剂的条件下,28gN2和6gH2充分反应,生成NH3的分子数为2NA |
