题目内容
8.三草酸合铁酸钾晶体K3[Fe(C2O4)3]•3H2O可用于摄影和蓝色印刷;已知草酸受热易分解产生CO2和CO.某小组将无水三草酸合铁酸钾按如图所示装置进行实验: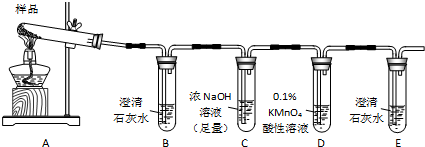
(1)若实验中,观察到B、E中溶液均变浑浊,则D中的现象是溶液褪色或变浅.
(2)你认为该实验设计还需要如何改进(请至少写出两处)①在AB装置之间加一个防倒吸装置;②在C装置后增加二氧化碳是否除净的检验装置(澄清石灰水);③最后缺少尾气处理装置.
(3)该小组同学查阅资料后推知,固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3.验证固体产物中钾元素存在的方法是利用焰色反应,现象是透过蓝色钴玻璃,观察到紫色的火焰.
(4)固体产物中铁元素存在形式的探究. ①提出合理假设:
假设1:只有Fe;
假设2:只有FeO;
假设3:含有Fe和FeO.
②设计实验方案并实验验证
步骤1:取适量固体产物于试管中,加入足量蒸馏水溶解,过滤分离出不溶固体.
步骤2:取少量上述不溶固体放人试管中,加入足量CuSO4溶液,充分振荡.若固体无明显变化,则假设2成立;若有红色固体生成,则反应的离子方程式为Fe+Cu2+=Cu+Fe2+.
步骤3:取步骤2所得固体于试管中,滴加过量HCl后,静置,取上层清液,滴加适量H2O2,充分振荡后滴加KSCN,振荡后静置.若溶液基本无色,则假设1成立;若溶液呈浅绿色,则假设3成立.
(5)拓展与延伸
有资料介绍“在含Fe2+的溶液中,先滴加少量新制饱和氯水,然后滴加KSCN溶液,溶液呈红色;若再滴加过量氯水,却发现红色褪去”.假设溶液中的+3价铁还能被氯水氧化为更高价的FeO42-,试写出该反应的离子方程式2Fe3++8H2O+3Cl2=2FeO42-+16H++6Cl-.
分析 装置A中无水三草酸合铁酸钾按受热分解,通过装置B中澄清石灰水,检验二氧化碳生成,装置C吸收二氧化碳,装置D为高锰酸钾溶液为强氧化剂,若实验中,观察到B、E中溶液均变浑浊,则D中的现象是溶液褪色或变浅,
(1)高锰酸钾具有氧化性,其溶液为紫红色,被还原性的物质还原溶液颜色变浅或褪色;
(2)检验产生的气体中含有CO、CO2,应该先通过澄清石灰水检验二氧化碳,但反应中可能导致B装置中的液体倒吸到A加热装置,产物CO有毒,需尾气处理,在C装置后增加二氧化碳是否除净的检验装置(澄清石灰水);
(3)钾离子的检验采用焰色反应来检验;
(4)①依据信息:固体产物中,铁元素不可能以三价形式存在,可推测铁元素只能以亚铁及铁单质的形式存在;
②用过量硫酸铜溶液检验金属铁的存在情况;由于硫酸铜过量,铁完全反应,利用盐酸溶解骤2所得暗红色固体,根据反应现象判断铁元素的存在形式;
(5)根据反应为铁离子和氯气,生成物FeO42-写出反应的离子方程式.
解答 解:(1)实验中,观察到B中溶液均变浑浊,说明无水三草酸合铁酸钾受热分解生成二氧化碳,E中溶液均变浑浊,说明经过具有氧化性的高锰酸钾溶液生成二氧化碳,所以还原性气体和高锰酸钾发生氧化还原反应,其溶液由紫红色变浅或褪色,
故答案为:溶液褪色或变浅;
(2)检验产生的气体中含有CO、CO2,应该先通过澄清石灰水检验二氧化碳,但反应流程装置中可能导致B装置中的液体倒吸到A加热装置,产物CO有毒,需尾气处理,在C装置后增加二氧化碳是否除净的检验装置(澄清石灰水),
故答案为:在AB装置之间加一个防倒吸装置;在C装置后增加二氧化碳是否除净的检验装置(澄清石灰水);最后缺少尾气处理装置;
(3)可以验证钾离子来确定是否存在碳酸钾,钾离子的检验可以用焰色反应法,
故答案为:利用焰色反应;透过蓝色钴玻璃,观察到紫色的火焰;
(4)①根据题意“固体产物中,铁元素不可能以三价形式存在”,所以存在的可能是零价铁或亚铁,可能情况有三种:只有Fe;只有FeO;含有Fe和FeO,
故答案为:含有Fe和FeO;
②步骤2:金属铁不溶于水中,但是可以和硫酸铜发生置换反应,生成金属铜和硫酸亚铁,所以取少置上述不溶固体放入试管中,加入足量CuSO4溶液,若蓝色溶液颜色及加入的不溶固体无明显变化,则假设2成立;若蓝色溶液颜色明显改变,且有暗红色固体生成,则证明有铁单质存在,发生反应的离子方程式为:Fe+Cu2+=Cu+Fe2+,
故答案为:CuSO4;2;Fe+Cu2+=Cu+Fe2+;
步骤3:氧化亚铁不溶于水,可以和盐酸反应生成氯化冶铁和水,可以检验亚铁离子的存在进而确定氧化亚铁的存在,方法为:取取步骤2所得暗红色固体于试管中,滴加过量HCl,静置,振荡后静置.若溶液基本无色,则假设1成立;若溶液呈浅绿色,则证明假设3成立,
故答案为:1;浅绿色;
(5)根据信息可知,铁离子被氯气氧化成FeO42-,根据化合价升降相等配平,配平后的离子方程式为:2Fe3++8H2O+3Cl2=2FeO42-+16H++6Cl-,
故答案为:2Fe3++8H2O+3Cl2=2FeO42-+16H++6Cl-.
点评 本题考查学生对元素及其化合物性质的掌握、对物质进行检验的实验技能,题目难度中等,有利于提高学生运用相关知识对实验提出假设及设计方案的能力.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 该酒在55℃的条件下酿造 | B. | 该酒的沸点为55℃ | ||
| C. | 100mL该酒中含乙醇55mL | D. | 100g该酒中含乙醇55g |
| A. | (NH4)2SO4 | B. | Cl2 | C. | NH3 | D. | CH3COOH |
| A. | 、萃取 | B. | 蒸馏 | C. | 分液 | D. | 过滤 |
| A. | 醋酸钠 | B. | 硝酸钾 | C. | 硫酸铵 | D. | 硫酸铜 |
| A. | “类钫”在化合物中呈+1价 | |
| B. | 类钫具有放射性 | |
| C. | 单质与水反应较为缓慢 | |
| D. | 类钫最高价氧化物对应的水化物是强碱 |