题目内容
14.核反应堆中存在三种具有放射性的微粒${\;}_{94}^{238}$X、${\;}_{94}^{240}$Y、${\;}_{92}^{238}$Z,下列说法正确的是( )| A. | ${\;}_{94}^{238}$X与${\;}_{94}^{240}$Y互为同素异形体 | |
| B. | ${\;}_{94}^{238}$X与${\;}_{92}^{238}$Z互为同素异形体 | |
| C. | ${\;}_{94}^{240}$Y与${\;}_{92}^{238}$Z具有相同中子数 | |
| D. | ${\;}_{94}^{238}$X与${\;}_{92}^{238}$Z具有相同化学性质 |
分析 同一元素的不同单质互称同素异形体;元素左上角数字表示质量数,中子数=质量数-质子数;元素的化学性质主要和原子的最外层电子数有关.
解答 解:A.${\;}_{94}^{238}$X与${\;}_{94}^{240}$Y是原子不是单质,不为同素异形体,故A错误;
B.${\;}_{94}^{238}$X与${\;}_{92}^{238}$Z是原子不是单质,不为同素异形体,故B错误;
C.中子数=质量数-质子数,${\;}_{94}^{240}$Y与${\;}_{92}^{238}$Z具有相同中子数,都为46,故C正确;
D.${\;}_{94}^{238}$X与${\;}_{92}^{238}$Z是不同元素,最外层电子数不同,化学性质不同,故D错误.
故选C.
点评 本题考查原子中的数量关系,明确质子数、中子数、质量数的关系,质子数与电子数的关系以及同位素、同素异形体的概念及判断是解答关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
4.已知X、Y为同周期主族元素,且电负性x>Y,下列说法一定错误的是( )
| A. | 原子半径:X<Y | |
| B. | 第一电离能:X>Y | |
| C. | 气态氢化物的稳定性:HmY小于HnY | |
| D. | X与Y形成化合物时,一般显负价,Y显正价 |
5.下列反应的离子方程式书写正确的是( )
| A. | 石灰石与盐酸反应:CO32ˉ+2H+═H2O+CO2↑ | |
| B. | 稀硫酸溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| C. | 铁粉与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 稀硫酸与氢氧化钠溶液反应:H++OHˉ═H2O |
2.现榨的苹果汁在空气中会由淡绿色变为棕黄色,其原因可能是( )
| A. | 苹果汁中的Fe2+变成Fe3+ | B. | 苹果汁中含有Cu2+ | ||
| C. | 苹果汁含有OH- | D. | 苹果汁含有Fe3+ |
19.硅与某非金属元素X的化合物具有高熔点高硬度的性能,X一定不可能是( )
| A. | ⅣA族元素 | B. | ⅤA族元素 | C. | ⅥA 族元素 | D. | ⅦA族元素 |
6.a、b、c、d四种短周期元素在周期表中分布如图所示,下列说法正确的是( )


| A. | 若四种元素均为主族元素,则d元素的原子半径最大 | |
| B. | 若b最外层电子占据三条轨道,则a的单质可用于冶炼金属 | |
| C. | 若a为非金属元素,则c的气态氢化物的水溶液可能呈碱性 | |
| D. | 若a最外层有两个未成对电子,则d的单质常温下不可能为气体 |
3.钛(Ti)金属常被称为未来钢铁,${\;}_{22}^{46}$Ti和${\;}_{22}^{47}$Ti是钛的两种同位素.下列有关Ti的说法正确的是( )
| A. | ${\;}_{22}^{46}$Ti比${\;}_{22}^{47}$Ti少1个质子 | |
| B. | ${\;}_{22}^{46}$Ti和${\;}_{22}^{47}$Ti的化学性质相同 | |
| C. | ${\;}_{22}^{46}$Ti的相对原子质量是46 | |
| D. | ${\;}_{22}^{47}$Ti的原子序数为47 |


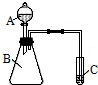 下表中实线表示目前元素周期表七个周期的部分边界. ①~⑧八种元素在周期表中的相对位置如下:
下表中实线表示目前元素周期表七个周期的部分边界. ①~⑧八种元素在周期表中的相对位置如下:
 .
.