题目内容
已知在酸性溶液中的还原性强弱顺序为:SO2>I->H2O2>Fe2+>Cl-,下列反应不可能发生的是( )
| A、2I-+2Fe3+=I2+2Fe2+ |
| B、2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
| C、SO2+2H2O+I2=H2SO4+2HI |
| D、H2O2+H2SO4=SO2↑+O2↑+2H2O |
考点:氧化还原反应,氧化性、还原性强弱的比较
专题:氧化还原反应专题
分析:根据氧化还原反应中还原剂的还原性大于还原产物的还原性,利用酸性溶液中还原性强弱的顺序是SO2>I->H2O2>Fe2+>Cl-来判断反应能否发生.
解答:
解:A.碘离子的还原性大于亚铁离子,所以碘离子能和铁离子发生氧化还原反应,能发生,故A不选;
B.二氧化硫的还原性大于亚铁离子,所以二氧化硫能氧化铁离子生成亚铁离子,能发生,故B不选;
C.因该反应中S元素的化合价升高,I元素的化合价降低,则SO2为还原剂,还原性强弱为SO2>I-,与已知的还原性强弱一致,能发生,故C不选;
D.若该反应发生,S元素的化合价降低,O元素的化合价升高,则H2O2为还原剂,还原性强弱为H2O2>SO2,与已知的还原性强弱矛盾,不可能发生,故D选.
故选D.
B.二氧化硫的还原性大于亚铁离子,所以二氧化硫能氧化铁离子生成亚铁离子,能发生,故B不选;
C.因该反应中S元素的化合价升高,I元素的化合价降低,则SO2为还原剂,还原性强弱为SO2>I-,与已知的还原性强弱一致,能发生,故C不选;
D.若该反应发生,S元素的化合价降低,O元素的化合价升高,则H2O2为还原剂,还原性强弱为H2O2>SO2,与已知的还原性强弱矛盾,不可能发生,故D选.
故选D.
点评:本题考查学生利用已知的还原性强弱来判断化学反应的发生,侧重于学生的分析能力的考查,注意应学会利用化合价来分析反应中的还原剂,并利用还原剂的还原性大于还原产物的还原性来解答即可,难度不大.

练习册系列答案
相关题目
25℃时,将0.2mol?L-1的HF加水稀释过程中,下列表示的量保持不变的是( )
①n(H+); ②c(H+)?c(OH-);③c(OH-)+c(F-);④
⑤
.
①n(H+); ②c(H+)?c(OH-);③c(OH-)+c(F-);④
| c(H+) |
| c(HF) |
| c(H+)?c(F-) |
| c(HF) |
| A、①③④ | B、②③④ |
| C、③④⑤ | D、②⑤ |
科学家刚刚发现了某种元素的一个原子,其质量是ag,12C的一个原子质量是bg,NA是阿伏伽德罗常数的值,下列说法正确的是( )
| A、该原子的摩尔质量是:aNA | ||
B、Wg该原子的物质的量是:
| ||
C、Wg该原子中含有
| ||
D、由已知信息可得:NA=
|
H-是负一价的阴离子,它可与NH3发生以下反应:H-+NH3=H2+NH2-,下列有关这个反应的说法中正确的是( )
| A、它属于置换反应 |
| B、该反应中NH2-是还原产物 |
| C、该反应中NH3被氧化 |
| D、反应中被氧化和被还原的元素都是H元素 |
将30mL0.5mol/LNaOH溶液加水稀释到500mL,稀释后溶液的浓度为( )
| A、0.1mol/L |
| B、0.3mol/L |
| C、0.05mol/L |
| D、0.03mol/L |
已知0.5LFe2(SO4)3溶液中Fe3+为1mol/L,则下列说法正确的是( )
| A、SO42-浓度为3mol/L |
| B、Fe3+的质量为28g |
| C、Fe2(SO4)3浓度为1mol/L |
| D、SO42-为0.5mol |
NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、7.8 gNa2O2与足量的水反应,转移的电子数为0.1NA |
| B、用含有0.1molFeCl3的饱和溶液制得的氢氧化铁胶体中,胶粒数等于0.1NA |
| C、25℃时,pH=13的1LBa(OH)2溶液中含有的OH-数为0.2NA |
| D、100mL 12 mol?L-1浓盐酸与足量MnO2加热反应,产生的氯气分子数为0.3NA |
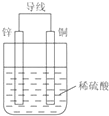 根据铜锌原电池示意图,回答下列问题:
根据铜锌原电池示意图,回答下列问题: