题目内容
将30mL0.5mol/LNaOH溶液加水稀释到500mL,稀释后溶液的浓度为( )
| A、0.1mol/L |
| B、0.3mol/L |
| C、0.05mol/L |
| D、0.03mol/L |
考点:物质的量浓度的相关计算
专题:
分析:根据稀释定律,稀释前后溶质NaOH的物质的量不变,据此计算稀释后溶液的浓度.
解答:
解:设稀释后NaOH的浓度为c,根据稀释定律,稀释前后溶质NaOH的物质的量不变,则:
0.03L×0.5mol/L=0.5L×c
解得c=0.03mol/L
故选D.
0.03L×0.5mol/L=0.5L×c
解得c=0.03mol/L
故选D.
点评:本题考查物质的量浓度有关计算,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
下列实验现象预测、实验设计、仪器使用能达到目的是( )
A、 模拟工业制氨气并检验产物 |
B、 分离沸点不同的两种液体 |
C、 收集并吸收多余氯气 |
D、 盛放浓硝酸 |
下列有关说法正确的是( )
| A、复分解反应一定都属于非氧化还原反应 |
| B、在氧化还原反应中,非金属单质一定是氧化剂 |
| C、某元素从化合物变为单质时,该元素一定被还原 |
| D、金属阳离子被还原一定得到金属单质 |
已知在酸性溶液中的还原性强弱顺序为:SO2>I->H2O2>Fe2+>Cl-,下列反应不可能发生的是( )
| A、2I-+2Fe3+=I2+2Fe2+ |
| B、2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
| C、SO2+2H2O+I2=H2SO4+2HI |
| D、H2O2+H2SO4=SO2↑+O2↑+2H2O |
下列说法正确的是:( )
| A、1mol蔗糖可水解生成2mol葡萄糖 |
| B、CH3-CH=CH-CH3与C3H6一定互为同系物 |
C、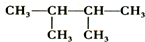 的名称是2,3-甲基丁烷 的名称是2,3-甲基丁烷 |
| D、乙醇可与水以任意比例混溶,是因为相似相溶原理且与水形成了氢键 |
由硫酸钠,硫酸铁和硫酸组成的混合液中,其c(H+)=0.1mol/L,c(Fe3+)=0.4mol/L,c(SO42-)=0.8mol/L,则c(Na+)为( )
| A、0.3mol/L |
| B、0.15mol/L |
| C、0.2mol/L |
| D、0.4mol/L |
 在a mL醋酸溶液中滴加0.01mol?L-1的氢氧化钠溶液,滴定曲线如图所示.
在a mL醋酸溶液中滴加0.01mol?L-1的氢氧化钠溶液,滴定曲线如图所示.