题目内容
已知 H2(g)+Br2(l)=2HBr(g)△H=-72kJ/mol,蒸发1molBr2(l)需要吸收的能量为30kJ,其它相关数据如下表:则表中a为( )
| H2(g) | Br2(g) | HBr(g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
| A、200 | B、230 |
| C、260 | D、404 |
考点:有关反应热的计算
专题:化学反应中的能量变化
分析:根据盖斯定律计算反应H2(g)+Br2(g)=2HBr(g)的△H=-72kJ/mol,结合△H=反应物的总键能-生成物的总键能列方程计算.
解答:
解:在H2(g)+Br2(l)=2HBr(g)△H=-72kJ/mol反应中,1mol Br2(g)液化放出的能量为30kJ,即Br2(g)=Br2(l)△H=-30kJ/mol,则H2(g)+Br2(g)=2HBr(g)△H=-102kJ/mol,反应热等于反应物的总键能减生成物的总键能,则△H=-102=436+a-2×369,a=200,
故选A.
故选A.
点评:本题考查反应热的有关计算、键能与反应热的关系等,题目难度中等,明确△H=反应物的总键能-生成物的总键能是解题的关键,注意反应热与键能的计算关系以及物质的不同聚集状态的转化.

练习册系列答案
相关题目
下列图象分别表示有关反应的反应过程与能量变化的关系 据此判断下列说法正确的是( )
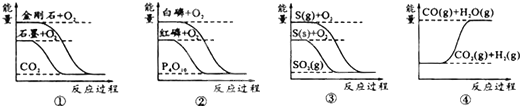

| A、石墨转变为金刚石是吸热反应 |
| B、白磷比红磷稳定 |
| C、CO (g)+H2O (g)=CO2 (g)+H2 (g)△H<0 |
| D、S (g)+O2 (g)=SO2 (g)△H1; S (s)+O2 (g)=SO2 (g)△H2,则△H1>△H2 |
在一定条件下发生如下反应:2KClO3+I2=2KIO3+Cl2,则下列推断不正确的是( )
| A、该反应属于置换反应 |
| B、该反应中KClO3被还原为Cl2 |
| C、该反应中氧化剂为KClO3 |
| D、该反应中氧化剂为I2 |
表中元素均为中学化学中常见短周期元素,根据表中信息,下列说法不正确的是( )
| 元素代号 | X | Y | Z | W | N |
| 原子半径/nm | 0.186 | 0.074 | 0.102 | 0.099 | 0.160 |
| 主要化合价 | +1 | -2 | -2、+6 | +7、-1 | +2 |
| A、常温下单质与水反应速率:X>N |
| B、最高价氧化物对应水化物酸性:W>Z |
| C、X 与W形成的化合物是共价化合物 |
| D、X和Y的单质在一定条件下反应可生成一种淡黄色的固体化合物 |
欲使0.1mol?L-1 的NaHSO3溶液中c(H+)、c(SO32-)都减少,其方法是( )
| A、加入过量CaO(s) |
| B、加入少量NaOH(s) |
| C、通入过量HCl(g) |
| D、加入少量H2O2 |
0.5mol H2含有( )
| A、0.5 mol 个氢气分子 |
| B、6.02×1023个氢气分子 |
| C、3.01×1023个氢气分子 |
| D、3.01×1023个电子 |
某气体的摩尔质量为M g?mol-1,NA表示阿伏加德罗常数,在一定的温度和压强下,体积为V L的该气体所含有的分子数为x.则
表示的是( )
| Mx |
| VNA |
| A、V L该气体的质量(以g为单位) |
| B、1 L该气体的质量(以g为单位) |
| C、1 mol该气体的体积(以L为单位) |
| D、1 L该气体中所含的分子数 |
 ③CH3CH2OH ④CH3COOH ⑤聚乙烯五种物质中:
③CH3CH2OH ④CH3COOH ⑤聚乙烯五种物质中: