题目内容
1.配制500mL 0.25mol/L的NaOH溶液,试回答下列问题:(1)计算
(2)某学生用托盘天平称量一个小烧杯的质量,称量前把游码放在标尺的零刻度处,天平静止时发现指针在分度盘的偏右位置,此时左边的托盘将高于(填“高于”或“低于”)右边的托盘.欲使天平平衡,所进行的操作为将左边的平衡螺母左旋移动,或将右边的平衡螺母左旋,直至天平平衡
(3)配制方法:某同学设计了四个操作步骤:
①向盛有NaOH的烧杯中加入200mL蒸馏水使其溶解,并冷却至室温.
②将NaOH溶液沿玻璃棒注入500mL容量瓶中.
③继续往容量瓶中加蒸馏水至液面接近刻度线1~2cm.
④改用胶头滴管加蒸馏水至刻度线,加盖摇匀.
若按上述步骤配制溶液物质的量浓度会偏低(填“偏高”或“偏低”或“无影响”).
分析 (2)分度盘的指针偏右,说明右边重,将左边的横梁螺丝往外调调节平衡;根据使用托盘天平时,加砝码的正确操作完成;
(3)该同学漏掉洗涤操作,导致部分溶质损耗,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(2)分度盘的指针偏右,说明右边重,左盘高于右盘.应将将左边的平衡螺母左旋移动,或将右边的平衡螺母左旋,直至天平平衡;
故答案为:高于;将左边的平衡螺母左旋移动,或将右边的平衡螺母左旋,直至天平平衡;
(3)该同学漏掉洗涤操作,导致部分溶质损耗,依据C=$\frac{n}{V}$可知溶液浓度偏低;
故答案为:偏低.
点评 本题以一定物质的量浓度溶液的配制为载体考查了托盘天平的使用方法和溶液配制误差分析的方法,熟悉托盘天平工作原理、明确不当操作对溶质的物质的量和溶液体积的影响是解题关键,题目难度不大.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
12.下列表示对应化学反应的离子方程式正确的是( )
| A. | 向NH4HCO3溶液中加入少量的Ba(OH)2溶液并加热:Ba2++2OH-+NH4++HCO3-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+2H2O+BaCO3↓ | |
| B. | 电解氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 少量CO2通入苯酚钠溶液:2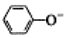 +CO2+H2O→2 +CO2+H2O→2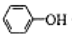 +CO32- +CO32- | |
| D. | 向明矾溶液中滴加Ba(OH)2溶液至溶液呈中性:2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ |
6.下列因果关系叙述正确的是( )
| A. | 浓硝酸中的HNO3见光会分解,因此有时在实验室看到的浓硝酸呈黄色 | |
| B. | SO2具有漂白性,因此可使溴水褪色 | |
| C. | Na的金属性比Cu强,因此可用Na与CuSO4溶液反应制取Cu | |
| D. | Fe在Cl2中燃烧生成FeCl3,因此在与其他非金属反应的产物中Fe也显+3价 |
13.下列说法正确的是( )
| A. | “雨后彩虹”是与胶体、光学等知识有关的自然现象 | |
| B. | “百炼成钢”主要发生了物理变化 | |
| C. | “返青粽叶”指的是添加胆矾(CuSO4•5H2O)后的粽叶青绿新鲜,长期食用有害健康,其中胆矾是混合物 | |
| D. | “明矾净水”与漂白粉用于自来水消毒的原理相同 |
11.下列说法正确的是( )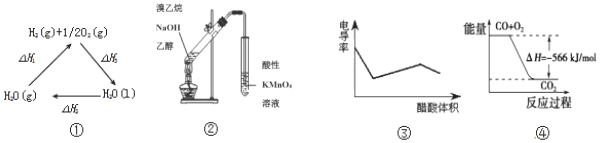

| A. | 图①中△H1=△H2+△H3 | |
| B. | 图②可用于证明实验中生成了乙烯 | |
| C. | 图③表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲线 | |
| D. | 图④可表示由CO(g)生成CO2(g)的过程中要放出566kJ 热量 |