题目内容
1.氯气是一种重要的化工原料.(1)氯水中含有多种成分,因而具有多种性质,新制氯水所含的微粒总共有7种,它们是Cl2、H2O、HClO、H+、Cl-、ClO-、OH-
(2)氯气是一种黄绿色非金属气体,化学性质上和氧气有许多相似之处,比如:氯气也能支持燃烧,写出铁丝在氯气中燃烧的方程式:2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3
(3)实验室制备氯气的化学方程式为MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
分析 (1)氯气和水的反应为Cl2+H2O?HCl+HClO,氯水中的成分为Cl2、H2O、HClO、H+、Cl-、ClO-、OH-;
(2)氯气是非金属单质,具有强氧化性,具有非金属单质的通性,可以和金属、非金属单质发生反应,铁在氯气中燃烧生成氯化铁;
(3)实验室利用二氧化锰做氧化剂和还原剂浓盐酸加热反应生成二氧化锰、氯气和水.
解答 解:(1)氯气和水的反应为Cl2+H2O?HCl+HClO,氯水中的成分为Cl2、H2O、HClO、H+、Cl-、ClO-、OH-,故答案为:Cl2、H2O、HClO、H+、Cl-、ClO-、OH-;
(2)铁在氯气中燃烧生成氯化铁,形成红褐色的烟,反应的化学方程式为:2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3,故答案为:2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3;
(3)实验室利用二氧化锰做氧化剂和还原剂浓盐酸加热反应生成二氧化锰、氯气和水,反应的化学方程式为MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
点评 本题考查氯气的性质,题目难度不大,注意氯水的成分和性质,化学方程式书写,注重基础知识的积累.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
11.某金属最高价氟化物的相对分子质量为M1,其最高价的硫酸盐的相对分子质量为M2,若此元素的最高正价为n,则n与M1、M2的关系可能是( )
| A. | n=$\frac{{M}_{2}-2{M}_{1}}{58}$ | B. | n=$\frac{{M}_{2}-{M}_{1}}{29}$ | C. | n=$\frac{2{M}_{2}-{M}_{1}}{58}$ | D. | n=$\frac{{M}_{2}-{M}_{1}}{58}$ |
12.下列关于醛的说法中正确的是( )
| A. | 所有醛中都含醛基和烃基 | |
| B. | 一元醛的分子式符合CnH2nO的通式 | |
| C. | 醛的官能团是-COH | |
| D. | 所有醛都能使溴水和酸性KMnO4溶液褪色 |
9.乙醚是化工生产中重要的溶剂,也用作药物生产的萃取剂和医疗上的麻醉剂.实验室通过乙醇脱水制备:
【原理】2CH3CH2OH$→_{140℃}^{浓H_{2}SO_{4}}$CH3CH2OCH2CH3+H2O
(170℃时产生CH2═CH2,长时间加热还会发生脱水、氧化还原反应等)
【主要物质物理性质】
【装置】
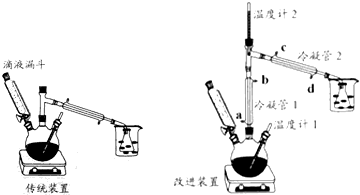
【实验步骤】
I、加浓硫酸和95%乙醇各12mL于三颈瓶中,并将三颈瓶浸入冰水中冷却,将25mL95%乙醇加入滴液漏斗,组装好仪器.
II、加热三颈瓶,使反应瓶温度迅速上升到140℃,然后开始慢慢滴加乙醇,控制合适的滴加速度,维持反应温度在135-145℃.
III、反应停止后,去掉热源,得粗产品.
IV、将粗产品转入仪器A,依次用8mL5%NaOH溶液、8mL试剂B、8mL(两次)饱和CaCl2溶液洗涤.
V、处理后的粗产品最后用无水氯化钙干燥至澄清,经操作C得到16.8g乙醚.
请回答:
(1)在步骤I中,向三颈瓶中加乙醇和浓硫酸的顺序是先加乙醇,再加浓硫酸.
(2)比较改进装置中两根冷凝管中水温的高低,如果用橡皮管将一个冷凝管的出水口接到另外一个冷凝管的进水口,有关说法和操作方法最合理的是B.
A、冷凝管1的水温相对高,水流方向为a→b→d→c
B、冷凝管1的水温相对高,水流方向为d→c→a→b
C、冷凝管2的水温相对高,水流方向为a→b→d→c
D、冷凝管2的水温相对高,水流方向为d→c→a→b
(3)反应过程中发现温度计1正常,温度计2的读数比预计温度高,为保证实验成功,可进行的操作是D.
A、适当加快滴液漏斗中乙醇的滴加速度 B、降低加热装置的加热温度
C、将温度计2拔高一点 D、加快冷凝管中水的流速
(4)改进装置能将产率提高50%,传统装置产率低的主要原因是传统装置中乙醇被大量蒸出,降低了产率.
(5)在步骤IV中,仪器A的名称是分液漏斗.
(6)在步骤IV中,用NaOH溶液时为了除去除去二氧化硫、二氧化碳,然后用试剂B洗涤NaOH,以免跟CaCl2产生沉淀,试剂B最好是饱和NaCl溶液(“乙醇”、“蒸馏水”、“饱和NaCl溶液”).
【原理】2CH3CH2OH$→_{140℃}^{浓H_{2}SO_{4}}$CH3CH2OCH2CH3+H2O
(170℃时产生CH2═CH2,长时间加热还会发生脱水、氧化还原反应等)
【主要物质物理性质】
| 物质 | 熔点℃ | 沸点℃ | 溶解性 | ||
| 水 | 醇 | 醚 | |||
| 浓硫酸 | 10.35 | 340 | 互溶 | 互溶 | 互溶 |
| 乙醚 | -89.12 | 34.5 | 微溶(在盐溶液中溶解度降低) | 互溶 | 互溶 |
| 乙醇 | -114.5 | 78.4 | 极易溶 | 极易溶 | 极易溶 |

【实验步骤】
I、加浓硫酸和95%乙醇各12mL于三颈瓶中,并将三颈瓶浸入冰水中冷却,将25mL95%乙醇加入滴液漏斗,组装好仪器.
II、加热三颈瓶,使反应瓶温度迅速上升到140℃,然后开始慢慢滴加乙醇,控制合适的滴加速度,维持反应温度在135-145℃.
III、反应停止后,去掉热源,得粗产品.
IV、将粗产品转入仪器A,依次用8mL5%NaOH溶液、8mL试剂B、8mL(两次)饱和CaCl2溶液洗涤.
V、处理后的粗产品最后用无水氯化钙干燥至澄清,经操作C得到16.8g乙醚.
请回答:
(1)在步骤I中,向三颈瓶中加乙醇和浓硫酸的顺序是先加乙醇,再加浓硫酸.
(2)比较改进装置中两根冷凝管中水温的高低,如果用橡皮管将一个冷凝管的出水口接到另外一个冷凝管的进水口,有关说法和操作方法最合理的是B.
A、冷凝管1的水温相对高,水流方向为a→b→d→c
B、冷凝管1的水温相对高,水流方向为d→c→a→b
C、冷凝管2的水温相对高,水流方向为a→b→d→c
D、冷凝管2的水温相对高,水流方向为d→c→a→b
(3)反应过程中发现温度计1正常,温度计2的读数比预计温度高,为保证实验成功,可进行的操作是D.
A、适当加快滴液漏斗中乙醇的滴加速度 B、降低加热装置的加热温度
C、将温度计2拔高一点 D、加快冷凝管中水的流速
(4)改进装置能将产率提高50%,传统装置产率低的主要原因是传统装置中乙醇被大量蒸出,降低了产率.
(5)在步骤IV中,仪器A的名称是分液漏斗.
(6)在步骤IV中,用NaOH溶液时为了除去除去二氧化硫、二氧化碳,然后用试剂B洗涤NaOH,以免跟CaCl2产生沉淀,试剂B最好是饱和NaCl溶液(“乙醇”、“蒸馏水”、“饱和NaCl溶液”).
16.下列反应的离子方程式正确的是( )
| A. | 向NaOH溶液中加入铝粉来制备H2:Al+2OH-+2H2O═AlO2-+3H2↑ | |
| B. | 碳酸钙溶于醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| C. | 实验室用氢氧化钠溶液吸收Cl2:Cl2+OH-═Cl-+ClO-+H2O | |
| D. | 用胃舒平治疗胃酸过多:Al(OH)3+3H+═Al3++3H2O |
6.下列有关电池的叙述正确的是( )
| A. | 锌锰干电池中,锌电极是负极 | |
| B. | 手机用的锂离子电池属于一次电池 | |
| C. | 太阳能电池的主要材料为二氧化硅 | |
| D. | 氢氧燃料电池工作时氢气在负极被还原 |
10.几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是( )
| 元素代号 | L | M | X | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
| A. | 氢化物的沸点为H2T<H2X | |
| B. | R的氧化物对应的水化物可能具有两性 | |
| C. | X单质在氧气中燃烧生成XO3 | |
| D. | L、X形成的简单离子核外电子数相等 |
11.如表为元素周期表的一部分.X、Y、Z、W为短周期元素,其中X元素的原子最外层电子数是其内层电子数的2倍.下列说法正确的是( )
| X | Y | ||
| Z | W | ||
| T |
| A. | 根据元素周期律,可以推测存在T3Y4、TZ2和TW4 | |
| B. | W的氧化物的水化物酸性一定比Z的强 | |
| C. | XZ2、XW4与YW3都是非极性分子 | |
| D. | X氢化物的沸点一定比Y氢化物的沸点低 |