题目内容
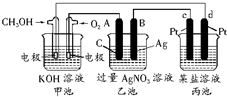 如图所示的装置中,甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.
如图所示的装置中,甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.试回答下列问题:
(1)图中甲池通入CH3OH电极的名称是
(2)写出通入CH3OH的电极的电极反应式:
(3)乙池中反应的化学方程式为
(4)乙池中盛有盛500mL 2mol/L AgNO3溶液,当 B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3.
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)甲装置为燃料电池,A与原电池的正极相连;
(2)燃料电池中燃料失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水;B电极与原电池负极相连,为阴极,银离子在B上得电子;
(3)乙为电解池,电解质溶液为AgNO3;
(4)根据电极方程式和电池反应结合电子守恒来计算.
(2)燃料电池中燃料失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水;B电极与原电池负极相连,为阴极,银离子在B上得电子;
(3)乙为电解池,电解质溶液为AgNO3;
(4)根据电极方程式和电池反应结合电子守恒来计算.
解答:
解:(1)甲装置为甲醇燃料电池,属于原电池,通入氧气的电极是正极,通入CH3OH电极是负极,A与原电池的正极相连,则A为阳极,B是阴极,c是阳极,d是阴极;
故答案为:负极;阳极;
(2)燃料电池中燃料失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水,其电极的电极反应式是CH3OH-6e-+8OH-═6H2O+CO32-;故答案为:CH3OH-6e-+8OH-═6H2O+CO32-;Ag++e-=Ag;
(3)乙为电解池,电解质溶液为AgNO3,则乙池中反应的化学方程式为4AgNO3+2H2O
4Ag+O2↑+4HNO3,
故答案为:4AgNO3+2H2O
4Ag+O2↑+4HNO3;
(4)乙池中A(Ag)极上银离子得电子生成Ag,其电极反应为Ag++e-=Ag,已知A(Ag)极的质量增加5.40g时,n(Ag)=
=0.05mol,
则转移电子为0.05mol,甲中正极反应为:O2+4e-+H2O=4OH-,则转移0.05mol电子时消耗的氧气为0.05mol×
=0.0125mol,则氧气的体积为0.0125mol×22.4L/mol=0.28L=280ml,乙池中的电池反应:4AgNO3+2H2O
4Ag+O2↑+4HNO3,当生成银0.05mol时,生成的硝酸的物质的量是0.05mol,所以硝酸的浓度是
=0.1mol/L,此时溶液的pH 是1,丙池某电极析出1.60g某金属,转移电子是0.05mol,只能是铜离子得电子析出金属铜,只有B符合,
故答案为:280;1;B.
故答案为:负极;阳极;
(2)燃料电池中燃料失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水,其电极的电极反应式是CH3OH-6e-+8OH-═6H2O+CO32-;故答案为:CH3OH-6e-+8OH-═6H2O+CO32-;Ag++e-=Ag;
(3)乙为电解池,电解质溶液为AgNO3,则乙池中反应的化学方程式为4AgNO3+2H2O
| ||
故答案为:4AgNO3+2H2O
| ||
(4)乙池中A(Ag)极上银离子得电子生成Ag,其电极反应为Ag++e-=Ag,已知A(Ag)极的质量增加5.40g时,n(Ag)=
| 5.4g |
| 108g/mol |
则转移电子为0.05mol,甲中正极反应为:O2+4e-+H2O=4OH-,则转移0.05mol电子时消耗的氧气为0.05mol×
| 1 |
| 4 |
| ||
| 0.05mol |
| 0.5L |
故答案为:280;1;B.
点评:本题考查了原电池和电解池原理,明确离子放电顺序是解本题关键,难点是电极反应式的书写,题目难度中等.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
已知aL硫酸铝溶液中,含有27g A13+,取0.5aL硫酸铝溶液稀释至2aL,则稀释后溶液中SO42ˉ的物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
150℃时,某白色固体完全分解为NH3、H2O、CO2三种物质,此时该混合气对氢气的相对密度为12.7,则( )
| A、该白色粉末为NH4HCO3 |
| B、该白色粉末为(NH4)2CO3 |
| C、该白色粉末为NH4HCO3与(NH4)2CO3 混合物且物质的量之比为1:2 |
| D、该白色粉末为NH4HCO3与(NH4)2CO3 混合物且物质的量之比为2:1 |
下列反应活化能最小的是( )
| A、2H2+O2=2H2O |
| B、3H2+O3=3H2O |
| C、2H+O=H2O |
| D、H2+Cl2=2HCl |
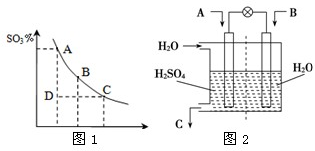 已知CO2、SO2、NOx是对环境影响较大的气体,请你运用所学知识参与环境治理,使我们周围的空气更好.
已知CO2、SO2、NOx是对环境影响较大的气体,请你运用所学知识参与环境治理,使我们周围的空气更好.