题目内容
(1)明矾晶体可用来净水,它的化学式为 .
(2)反应KClO3+6HCl=KCl+3Cl2↑+3H2O 中氧化剂是 ,氧化剂和还原剂的物质的量之比 .
(3)加热10.0g碳酸钠和碳酸氢钠的混合物至质量不在变化,剩余固体的质量为8.45g,则混合物中碳酸钠的质量分数为 . (填能或者不能)用澄清石灰水鉴别碳酸钠和碳酸氢钠溶液.
(4)等物质的量浓度的NaCl、MgCl2、AlCl3溶液与足量的AgNO3溶液完全反应,若产生相同质量的沉淀,则消耗NaCl、MgCl2、AlCl3溶液的体积之比为 .
(2)反应KClO3+6HCl=KCl+3Cl2↑+3H2O 中氧化剂是
(3)加热10.0g碳酸钠和碳酸氢钠的混合物至质量不在变化,剩余固体的质量为8.45g,则混合物中碳酸钠的质量分数为
(4)等物质的量浓度的NaCl、MgCl2、AlCl3溶液与足量的AgNO3溶液完全反应,若产生相同质量的沉淀,则消耗NaCl、MgCl2、AlCl3溶液的体积之比为
考点:氧化还原反应,化学方程式的有关计算,钠的重要化合物
专题:计算题,氧化还原反应专题,元素及其化合物
分析:(1)明矾为十二水硫酸铝钾;
(2)KClO3+6HCl=KCl+3Cl2↑+3H2O中,Cl元素的化合价由+5价降低为0,Cl元素的化合价由-1价升高为0;
(3)加热碳酸钠和碳酸氢钠的混合物时,碳酸钠不分解,碳酸氢钠不稳定,加热时分解生成碳酸钠、二氧化碳和水,利用差量法,根据2NaHCO3
Na2CO3+CO2↑+H2O计算碳酸氢钠的质量,进而计算碳酸钠的质量分数;二者均与石灰水反应生成碳酸钙沉淀;
(4)产生相同质量的沉淀,则生成的AgCl相同,氯离子物质的量相同,浓度相同时,由n=cV可知,溶液的体积之比等于物质的量之比.
(2)KClO3+6HCl=KCl+3Cl2↑+3H2O中,Cl元素的化合价由+5价降低为0,Cl元素的化合价由-1价升高为0;
(3)加热碳酸钠和碳酸氢钠的混合物时,碳酸钠不分解,碳酸氢钠不稳定,加热时分解生成碳酸钠、二氧化碳和水,利用差量法,根据2NaHCO3
| ||
(4)产生相同质量的沉淀,则生成的AgCl相同,氯离子物质的量相同,浓度相同时,由n=cV可知,溶液的体积之比等于物质的量之比.
解答:
解:(1)明矾为十二水硫酸铝钾,化学式为KAl(SO4)2?12H2O,故答案为:KAl(SO4)2?12H2O;
(2)KClO3+6HCl=KCl+3Cl2↑+3H2O中,Cl元素的化合价由+5价降低为0,Cl元素的化合价由-1价升高为0,则KClO3为氧化剂,HCl为还原剂,5molHCl与1mol氧化剂转移电子守恒,则氧化剂和还原剂的物质的量之比为1:5,故答案为:KClO3;1:5;
(3)加热碳酸钠和碳酸氢钠的混合物时,碳酸钠不分解,碳酸氢钠不稳定,则固体质量减少的原因是由于碳酸氢钠分解的缘故,设混合物中碳酸氢钠的质量为m,
2NaHCO3
Na2CO3+CO2↑+H2O△m
2×84g 62g
m 10.0g-8.45g=1.55g
m=
=4.2g,
所以混合物中碳酸钠的质量为10.0g-4.2g=5.8g,
混合物中碳酸钠的质量分数为:
×100%=58%,
二者均与石灰水反应生成碳酸钙沉淀,现象相同,不能用澄清石灰水鉴别碳酸钠和碳酸氢钠溶液,
故答案为:58%;不能;
(4)产生相同质量的沉淀,则生成的AgCl相同,氯离子物质的量相同,浓度相同时,由n=cV可知,溶液的体积之比等于物质的量之比,设生成AgCl均为6mol,则NaCl、MgCl2、AlCl3的物质的量分别为6mol、3mol、2mol,则消耗NaCl、MgCl2、AlCl3溶液的体积之比为6:3:2,故答案为:6:3:2.
(2)KClO3+6HCl=KCl+3Cl2↑+3H2O中,Cl元素的化合价由+5价降低为0,Cl元素的化合价由-1价升高为0,则KClO3为氧化剂,HCl为还原剂,5molHCl与1mol氧化剂转移电子守恒,则氧化剂和还原剂的物质的量之比为1:5,故答案为:KClO3;1:5;
(3)加热碳酸钠和碳酸氢钠的混合物时,碳酸钠不分解,碳酸氢钠不稳定,则固体质量减少的原因是由于碳酸氢钠分解的缘故,设混合物中碳酸氢钠的质量为m,
2NaHCO3
| ||
2×84g 62g
m 10.0g-8.45g=1.55g
m=
| 2×84g×1.55g |
| 62g |
所以混合物中碳酸钠的质量为10.0g-4.2g=5.8g,
混合物中碳酸钠的质量分数为:
| 5.8g |
| 10.0g |
二者均与石灰水反应生成碳酸钙沉淀,现象相同,不能用澄清石灰水鉴别碳酸钠和碳酸氢钠溶液,
故答案为:58%;不能;
(4)产生相同质量的沉淀,则生成的AgCl相同,氯离子物质的量相同,浓度相同时,由n=cV可知,溶液的体积之比等于物质的量之比,设生成AgCl均为6mol,则NaCl、MgCl2、AlCl3的物质的量分别为6mol、3mol、2mol,则消耗NaCl、MgCl2、AlCl3溶液的体积之比为6:3:2,故答案为:6:3:2.
点评:本题考查较综合,涉及氧化还原反应、化学反应的计算及浓度的计算等,为高频考点,把握发生的反应、物质的性质及相关计算公式为解答的关键,侧重分析与计算能力及综合应用能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列溶液氯离子的物质的量浓度与50mL 2mol?L-1氯化铝溶液中氯离子的物质的量浓度相等的是( )
| A、150 mL 1 mol?L-1氯化钠溶液 |
| B、75 mL 1.5 mol?L-1氯化钙溶液 |
| C、150 mL 3 mol?L-1氯化钾溶液 |
| D、50 mL 3 mol?L-1氯化镁溶液 |
下列各图均能表示甲烷的分子结构,哪一种更能反映其真实存在状况( )
A、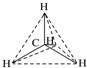 甲烷分子结构示意 |
B、 甲烷分子的电子 |
C、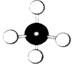 球棍模型 |
D、 比例模型 |
海水中含有MgCl2,从海水中提取镁,正确的方法是( )
A、海水
| ||||||
B、海水
| ||||||
C、海水
| ||||||
D、海水
|
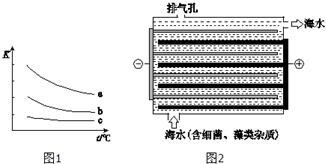 海水是巨大的化学资源宝库.
海水是巨大的化学资源宝库.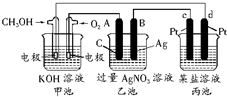 如图所示的装置中,甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.
如图所示的装置中,甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O. 的有机物,在核磁共振氢谱上吸收峰的面积之比为
的有机物,在核磁共振氢谱上吸收峰的面积之比为